Kobber og zinknitrat:Forståelse af den manglende reaktion
* Reaktivitetsserien: Kobber er mindre reaktivt end zink. Det betyder, at kobber ikke kan fortrænge zink fra sin saltopløsning.
* Elektrokemisk potentiale: Zink har et mere negativt standardelektrodepotentiale end kobber. Det betyder, at zink er mere tilbøjelige til at miste elektroner og blive oxideret, mens kobber er mere tilbøjelige til at få elektroner og blive reduceret.
Sammenfattende er reaktionen mellem kobber og zinknitrat ikke termodynamisk gunstig , og der vil ikke blive observeret nogen synlige ændringer.
Hvad ville der ske, hvis situationen blev vendt?
Hvis zinkmetal blev anbragt i en kobbernitratopløsning, ville der opstå en reaktion:
* Zink fortrænger kobber: Zink, der er mere reaktivt, ville fortrænge kobber fra opløsningen. Dette ville resultere i dannelsen af zinknitrat i opløsning og aflejring af fast kobbermetal på zinkoverfladen.
Ligning for reaktionen:
Zn(s) + Cu(NO3)₂(aq) → Zn(NO3)₂(aq) + Cu(s)
Sidste artikelKulstofisotoper:Forståelse af ¹²C, ¹³C og ¹⁴C
Næste artikelBronze:Forstå hvorfor det er en legering, ikke en homogen blanding
 Varme artikler
Varme artikler
-
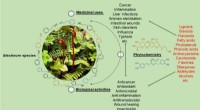 Forskere gennemgår anvendelser, fytokemi og farmakologiske egenskaber af slægten BlechnumMedicinsk anvendte Blechnum-planter. Kredit:WBG Flere værdifulde bregner, der tilhører slægten Blechnum, driver fra gård til traditionel helbredelse og etnofarmakologi, og er potentielle midler til
Forskere gennemgår anvendelser, fytokemi og farmakologiske egenskaber af slægten BlechnumMedicinsk anvendte Blechnum-planter. Kredit:WBG Flere værdifulde bregner, der tilhører slægten Blechnum, driver fra gård til traditionel helbredelse og etnofarmakologi, og er potentielle midler til -
 Forskere gør plastik mere nedbrydeligt under UV-lysKredit:Unsplash/CC0 Public Domain Mange plastiktyper, der er mærket som biologisk nedbrydelige, er kun komposterbare under industrielle forhold, men forskere ved University of Bath har nu fundet en
Forskere gør plastik mere nedbrydeligt under UV-lysKredit:Unsplash/CC0 Public Domain Mange plastiktyper, der er mærket som biologisk nedbrydelige, er kun komposterbare under industrielle forhold, men forskere ved University of Bath har nu fundet en -
 Hvad er bevaret i kemiske reaktioner? Forståelse af loven om bevaring af stofferAf David Dunning, opdateret 30. august 2022 Bevarelse af stof Kemiens grundlæggende princip, Loven om Materiens Bevarelse, siger, at stof ikke kan skabes eller ødelægges i et lukket system. I en typi
Hvad er bevaret i kemiske reaktioner? Forståelse af loven om bevaring af stofferAf David Dunning, opdateret 30. august 2022 Bevarelse af stof Kemiens grundlæggende princip, Loven om Materiens Bevarelse, siger, at stof ikke kan skabes eller ødelægges i et lukket system. I en typi -
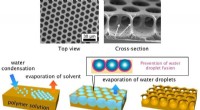 Ud af tågen:Honeycomb-filmSkematiske (nederst) og elektronmikrofotografier (øverst) af væksten af en honeycomb polystyrenfilm ved ånde-figur teknikken. Kredit:STAM Forskere producerer honeycomb-formede film ved hjælp af
Ud af tågen:Honeycomb-filmSkematiske (nederst) og elektronmikrofotografier (øverst) af væksten af en honeycomb polystyrenfilm ved ånde-figur teknikken. Kredit:STAM Forskere producerer honeycomb-formede film ved hjælp af
- Hvordan er sommeren på Uranus?
- Hvilke elementer fluor og klor kan danne mineraler i?
- Hvilke typer deformation gennemgår klipper under dannelse af et orogen bælte, såsom Alperne?
- Hvilken organisme er involveret i den mest nitrogenfikseringsjord?
- Forskere demonstrerer, at organiske krystaller kan tjene som energiomformere til nye teknologier
- Hvad er et specialiseret område af endoplasmatisk retikulum?


