Hvad er bevaret i kemiske reaktioner? Forståelse af loven om bevaring af stoffer
Af David Dunning, opdateret 30. august 2022
Bevarelse af stof
Kemiens grundlæggende princip, Loven om Materiens Bevarelse, siger, at stof ikke kan skabes eller ødelægges i et lukket system. I en typisk kemisk reaktion er den samlede masse af reaktanterne lig med den samlede masse af produkterne. Det betyder, at mængden af stof før og efter reaktionen forbliver konstant.
Illustrativt eksempel:Dannelse af vand
Overvej reaktionen af hydrogengas (H2) med oxygengas (O2) til dannelse af vand (H2O). Et mol vand indeholder to mol brint og et mol oxygen. I massetal reagerer 2,02 g brint med 16 g ilt og producerer 18,02 g vand, hvilket perfekt illustrerer bevarelsen af massen.
Bestemmelse af empiriske formler
Loven tillader også kemikere at udlede den empiriske formel for en ukendt forbindelse. Ved at måle massen af hvert element i en prøve og reducere de resulterende forhold til deres enkleste hele talform, kan den empiriske formel bestemmes.
Atomøkonomi og grøn kemi
Atomøkonomi refererer til den del af reaktantatomer, der ender i det ønskede produkt. Reaktioner med høj atomøkonomi omdanner det meste af udgangsmaterialet til nyttige produkter, hvilket genererer mindre affald. Sådanne processer er centrale for initiativer inden for grøn kemi, der sigter mod at reducere miljøbelastningen.
At forstå disse principper er afgørende for kemikere, ingeniører og alle, der arbejder med kemiske processer.
 Varme artikler
Varme artikler
-
 AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab
AI identificerer ændringer i mikrostruktur i aldrende materialerTopologisk analyse af røntgen-CT-data til genkendelse og trending af ændringer i mikrostruktur under materialeældning. Kredit:Lawrence Livermore National Laboratory Lawrence Livermore National Lab -
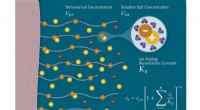 Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter
Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter -
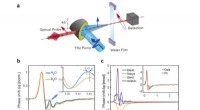 Ultrahurtig hydrogenbindingsdynamik af flydende vand afsløret af THz-induceret Kerr-effekten, Skematisk diagram af det eksperimentelle system. En bredbånds THz pumpeimpuls (peak elektrisk feltstyrke på 14,9 MV/cm, centerfrekvens på 3,9 THz, og båndbredde på 1-10 THz) exciterer flydende van
Ultrahurtig hydrogenbindingsdynamik af flydende vand afsløret af THz-induceret Kerr-effekten, Skematisk diagram af det eksperimentelle system. En bredbånds THz pumpeimpuls (peak elektrisk feltstyrke på 14,9 MV/cm, centerfrekvens på 3,9 THz, og båndbredde på 1-10 THz) exciterer flydende van -
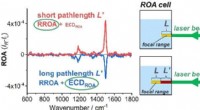 Interferens fører til unøjagtig Raman-spektroskopisk analyse af vitamin B12Kredit:Wiley Mange naturlige produkter er komplicerede organiske molekyler. På trods af denne kompleksitet, videnskabsmænd er normalt i stand til at undersøge dem ved hjælp af spektroskopiske tekn
Interferens fører til unøjagtig Raman-spektroskopisk analyse af vitamin B12Kredit:Wiley Mange naturlige produkter er komplicerede organiske molekyler. På trods af denne kompleksitet, videnskabsmænd er normalt i stand til at undersøge dem ved hjælp af spektroskopiske tekn
- Genetikens rolle i landbrugsproduktiviteten?
- Vestafrikanske piger viser vejen i Senegals teknologikamp
- Hvad er potentiel energi, der kaldes, der er forbundet med objekter, kan strækkes?
- Hvorfor udgør vandformigt hydrogenbindinger?
- Hvilken aminosyre findes i vandopløseligt kugleformet protein?
- Forsker viser global opvarmningseffekt på drivhusgasemissioner i uafskallet jord


