Mastering Moles in Chemistry:En praktisk guide til molar masse og støkiometri
Af Judy Tyler | Opdateret 30. august 2022
I kemi, en muldvarp er den grundlæggende enhed, der forbinder antallet af partikler til massen i støkiometriske ligninger. Et mol af ethvert stof indeholder nøjagtigt 6,02×10²³ atomer, ioner eller molekyler, en værdi kendt som Avogadros tal. Massen af en mol – kaldet den molære masse -er numerisk lig med grundstoffets massetal i gram. For forbindelser er molmassen summen af atommasserne af alle indgående atomer i de rigtige forhold.
Bestemmelse af et grundstofs molære masse
Trin 1 – Identificer elementet
Find lithium (Li) på det periodiske system. Dets atomnummer, 3, angiver antallet af protoner i hver kerne.
Trin 2 – Bemærk massenummeret
Lithiums massetal er 6,94, det kombinerede antal protoner og neutroner i dets kerne.
Trin 3 – Beregn molmassen
Fordi massetallet er lig med massen i gram af én mol, er lithiums molære masse 6,94 gmol⁻¹ .
Bestemmelse af en kemisk forbindelses molekylære masse
Trin 1 – Vælg sammensætningen
Vælg kuldioxid (CO₂) som eksempel. Identificer de indgående atomer - carbon og oxygen - i det periodiske system.
Trin 2 – Hent atommasser
Kulstof har en atommasse på 12,01 gmol⁻¹, og oxygen er 16,00 gmol⁻¹.
Trin 3 – Sum bidragene
Molekylmassen af CO₂ er beregnet som 12,01+2(16,00)=44,01gmol⁻¹ .
Konvertering fra masse til mol
Trin 1 – Identificer stoffet og massen
Bestem, hvor mange mol der er i 600 g vand (H₂O) . Bemærk, at vands molære masse er 18,02 gmol⁻¹.
Trin 2 – Konfigurer det proportionelle forhold
xmolH₂O=(1molH₂O/18,02gH₂O)×600gH₂O
Trin 3 – Løs for antallet af muldvarpe
Løsning af ligningen giver ≈33,3mol vand i 600 g af væsken.
Disse ligefremme beregninger danner grundlaget for nøjagtig støkiometrisk analyse og kvantitativ kemisk forskning.
 Varme artikler
Varme artikler
-
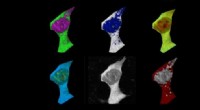 Alzheimers sygdom får celler til at overophedes og stege som ægPattedyrscelle farvet med fluorescens polymere termometre og falsk farvet baseret på temperaturgradienter. Kredit:Chyi Wei Chung Forskere har vist, at aggregering af amyloid-beta, et af to nøglepro
Alzheimers sygdom får celler til at overophedes og stege som ægPattedyrscelle farvet med fluorescens polymere termometre og falsk farvet baseret på temperaturgradienter. Kredit:Chyi Wei Chung Forskere har vist, at aggregering af amyloid-beta, et af to nøglepro -
 Forudsigelse af kemiske processer for at hjælpe landbrugsvirksomheder, kosmetik, brændstof- og fø…Vagtel forudsigelse af en koffein orbital i vand. Åbne grænseforhold afslører udvidede elektroniske tilstande – i modsætning til avancerede modeller. Quail Modelng LLC har udviklet software til bedre
Forudsigelse af kemiske processer for at hjælpe landbrugsvirksomheder, kosmetik, brændstof- og fø…Vagtel forudsigelse af en koffein orbital i vand. Åbne grænseforhold afslører udvidede elektroniske tilstande – i modsætning til avancerede modeller. Quail Modelng LLC har udviklet software til bedre -
 Video:Hvorfor plastikflasker genbruges til tøjKredit:The American Chemical Society Træningstøj og trendy håndtasker lavet af genbrugsplastik er i højsædet og hjælper forbrugerne med at føle, som om de gør deres del for miljøet. Men der er fle
Video:Hvorfor plastikflasker genbruges til tøjKredit:The American Chemical Society Træningstøj og trendy håndtasker lavet af genbrugsplastik er i højsædet og hjælper forbrugerne med at føle, som om de gør deres del for miljøet. Men der er fle -
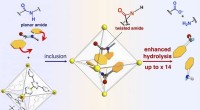 En molekylær trykkoger mører hårde stykker protein og hjælper med at bide afEt skema for reaktionshastighedsacceleration af amidhydrolyse ved inklusion i det selvsamlede molekylære bur. Kredit:NINS/IMS Proteiner består af aminosyrer forbundet med amidbindinger. Amidbindin
En molekylær trykkoger mører hårde stykker protein og hjælper med at bide afEt skema for reaktionshastighedsacceleration af amidhydrolyse ved inklusion i det selvsamlede molekylære bur. Kredit:NINS/IMS Proteiner består af aminosyrer forbundet med amidbindinger. Amidbindin
- Hvilket makromolekyle udgør et enzym?
- Hvilke atomer og hvor mange af hver er til stede i et vandmolekyle?
- Hvilke faktorer er nødvendige for at opretholde en stabil bane omkring himmelsk krop?
- Hvad hedder fabrikkerne denne proces elektricitet?
- Cassini udforsker ringlignende formationer omkring Titans søer
- Hvad er de vigtigste organsystemer i menneskets krop?


