Protoner i syre-basereaktioner:En detaljeret forklaring
Syrer:
* Doner protoner (H+): Syrer er stoffer, der frigiver hydrogenioner (H+), også kendt som protoner, når de er opløst i vand.
* Øg H+ koncentrationen: Tilstedeværelsen af flere protoner i opløsning gør opløsningen mere sur.
Baser:
* Accepter protoner (H+): Baser er stoffer, der accepterer protoner (H+), når de er opløst i vand.
* Reducer H+ koncentration: Baser fjerner protoner fra opløsningen, hvilket gør opløsningen mindre sur (mere basisk).
Blanding af syrer og baser:
* Neutraliseringsreaktion: Når en syre og en base reagerer, gennemgår de en neutraliseringsreaktion. Dette er en proces, hvor syrens protoner (H+) reagerer med basens hydroxidioner (OH-) og danner vand (H2O).
* Eksempel: HCl (syre) + NaOH (base) -> NaCl (salt) + H2O (vand)
* pH-ændring: Tilsætning af en syre til en base (eller omvendt) resulterer i en ændring i opløsningens pH.
* Syre + Base -> Mere neutral pH :Hvis syren og basen er i lige store mængder, neutraliserer de hinanden, hvilket resulterer i en neutral opløsning med en pH tæt på 7.
* Overskydende syre -> Lavere pH: Hvis der er et overskud af syre, vil opløsningen forblive sur med en lavere pH.
* Overskydende base -> Højere pH: Hvis der er et overskud af base, vil opløsningen blive mere basisk med en højere pH.
Nøglepunkter:
* Protoner er nøglespillerne i syre-base reaktioner.
* Syrer donerer protoner, baser accepterer dem.
* Neutralisering er en proces, hvor protoner og hydroxidioner kombineres for at danne vand.
* pH-værdien af en opløsning afspejler koncentrationen af protoner.
Sig til, hvis du vil have en mere detaljeret forklaring eller eksempler på specifikke syre-base reaktioner!
 Varme artikler
Varme artikler
-
 Ingeniører gør mikrofluidik modulopbygget ved hjælp af de populære sammenlåsende blokkeMIT -forskere har udviklet en ny platform for mikrofluidik, ved hjælp af LEGO klodser. Vist her, væske strømmer gennem bittesmå kanaler fræset ind i sidevæggene på LEGO klodser. Kredit:Massachusetts I
Ingeniører gør mikrofluidik modulopbygget ved hjælp af de populære sammenlåsende blokkeMIT -forskere har udviklet en ny platform for mikrofluidik, ved hjælp af LEGO klodser. Vist her, væske strømmer gennem bittesmå kanaler fræset ind i sidevæggene på LEGO klodser. Kredit:Massachusetts I -
 Multipel myrelignende transport af neuronal last med motorproteinerGodstransport med mange motorer gør neuronal aktivitet fin. Kredit:Kumiko Hayashi Mikrotubuli er veje lavet af proteiner, der strækker sig gennem en celle for motorproteiner (bærere) til at levere
Multipel myrelignende transport af neuronal last med motorproteinerGodstransport med mange motorer gør neuronal aktivitet fin. Kredit:Kumiko Hayashi Mikrotubuli er veje lavet af proteiner, der strækker sig gennem en celle for motorproteiner (bærere) til at levere -
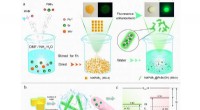 Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD
Blyhalogenid perovskiter med forbedret luminescens og stabiliteta) Skematisk diagram af synteseprocessen for MAPbBr3@PbBr(OH). b) Skematisk illustration af morfologiudviklingen af den fremstillede MAPbBr3-perovskit. c) Energiniveaudiagram af PbBr(OH) og indre QD -
 Plane og buede pyrrol-fusionerede azacoronerπ-Udvidet azacoronen med en Janus dobbeltkonkav struktur Credit:Graduate School of Science and Engineering, Ehime Universitet Nylige undersøgelser af syntetiske tilgange til polycykliske aromatisk
Plane og buede pyrrol-fusionerede azacoronerπ-Udvidet azacoronen med en Janus dobbeltkonkav struktur Credit:Graduate School of Science and Engineering, Ehime Universitet Nylige undersøgelser af syntetiske tilgange til polycykliske aromatisk
- Hvad er lagene af Jupiter?
- Hvilken form for energi frigives ikke, når neglen rammer en hammer?
- Trin-for-trin guide til sikker og præcis tilslutning af et amperemeter
- Hvorfor kunstig intelligens sandsynligvis vil tage flere liv
- Er det muligt at fremstille elektricitet gennem vejrtrækning - under udånding og indåndingsproces…
- Carpentry Compiler hjælper træarbejdere med at designe genstande, som de rent faktisk kan lave


