Forståelse af kemiske koefficienter:Forklaret støkiometri
Her er en oversigt:
* Hvad det repræsenterer: Koefficienten fortæller dig det støkiometriske forhold af reaktanterne og produkterne. Dette forhold repræsenterer det mindste antal molekyler (eller mol), der er nødvendige for, at reaktionen kan ske som skrevet.
* Sådan virker det: For eksempel i ligningen:
```
2 H2 + O2 -> 2 H20
```
* Koefficienten 2 foran H₂ betyder, at der kræves to mol hydrogengas (H2) til reaktionen.
* Koefficienten 1 (underforstået) foran O₂ betyder, at der er behov for et mol oxygengas (O₂).
* Koefficienten 2 foran H₂O angiver, at der produceres to mol vand (H2O).
Vigtige bemærkninger:
* Koefficienter er heltal kun. Du kan ikke have brøker som koefficienter i en afbalanceret kemisk ligning.
* De kan justeres at afbalancere den kemiske ligning og sikre, at antallet af atomer i hvert grundstof på begge sider af ligningen er ens.
* Koefficienter ændres ikke de kemiske formler for reaktanterne eller produkterne. De angiver kun de relative mængder af hvert stof involveret i reaktionen.
Forståelse af koefficienter er afgørende for:
* Forudsigelse af mængden af reaktanter og produkter involveret i en reaktion.
* Beregning af udbytte af produkter i kemiske reaktioner.
* Bestemmelse af den begrænsende reaktant i en reaktion.
Ved at justere koefficienter for at balancere en kemisk ligning sikrer vi, at loven om bevarelse af masse overholdes, som siger, at stof ikke kan skabes eller ødelægges i en kemisk reaktion.
 Varme artikler
Varme artikler
-
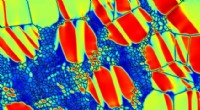 I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og
I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og -
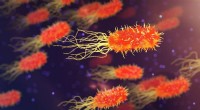 Strukturen af en bakteriel lægemiddelpumpe afslører en ny måde at modvirke hospitalsbåren infe…Kredit:CC0 Public Domain Ved at afsløre strukturen af et protein, der bruges af bakterier til at pumpe antibiotika ud, har et forskerhold designet et tidligt terapeutisk middel, der saboterer pum
Strukturen af en bakteriel lægemiddelpumpe afslører en ny måde at modvirke hospitalsbåren infe…Kredit:CC0 Public Domain Ved at afsløre strukturen af et protein, der bruges af bakterier til at pumpe antibiotika ud, har et forskerhold designet et tidligt terapeutisk middel, der saboterer pum -
 Hvordan muslinger laver en kraftig undervandslimMuslingernes skæg (som kogene fjerner, før de tilberedes) består af byssaltråde og bruges til at hjælpe med at holde muslingerne bundet på plads. For enden af hver tråd er en skiveformet plak, der f
Hvordan muslinger laver en kraftig undervandslimMuslingernes skæg (som kogene fjerner, før de tilberedes) består af byssaltråde og bruges til at hjælpe med at holde muslingerne bundet på plads. For enden af hver tråd er en skiveformet plak, der f -
 At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et
At finde kilden til kemiske reaktionerKredit:CC0 Public Domain Forskere søger konstant efter kilden til ting som universets oprindelse, materie eller liv. Forskere ved U.S. Department of Energys (DOE) Argonne National Laboratory, i et
- Hvad har mere momentum end en biltype friktion mellem stationære genstande?
- Lille lasersensor øger bombedetekteringsfølsomheden
- Hvad er videnskaben om forhold til ting og rum og rum?
- Havagurker:Opløsning af koralrev?
- Miljøødelæggelse er en krigsforbrydelse, men det er næsten umuligt at forfalde til lovene
- Hvilke husholdningsgenstande er ledere?


