Ionisk dissociation i vand:En omfattende forklaring
* Vands polaritet: Vand er et polært molekyle, hvilket betyder, at det har en let positiv ende (brint) og en lidt negativ ende (ilt).
* Ioniske forbindelser: Ioniske forbindelser er sammensat af positivt ladede ioner (kationer) og negativt ladede ioner (anioner) holdt sammen af elektrostatiske kræfter.
* Dissociation: Når en ionforbindelse er opløst i vand, omgiver de polære vandmolekyler ionerne. Den positive ende af vandmolekyler tiltrækker de negative ioner (anioner), mens den negative ende af vandmolekyler tiltrækker de positive ioner (kationer). Denne tiltrækning overvinder de elektrostatiske kræfter, der holder ionerne sammen i den faste forbindelse, hvilket får den ioniske forbindelse til at bryde fra hinanden eller dissociere til individuelle ioner.
Eksempel: Overvej bordsalt (NaCl). Når de er opløst i vand, adskilles natriumionerne (Na+) og chloridionerne (Cl-) fra hinanden.
Nøglepunkter:
* Ikke alle ioniske forbindelser er lige opløselige i vand: Nogle ioniske forbindelser er mere opløselige end andre, afhængigt af styrken af de elektrostatiske kræfter, der holder dem sammen, og interaktionen med vandmolekyler.
* Dissociation er ikke det samme som ionisering: Dissociation refererer til adskillelsen af eksisterende ioner i en forbindelse, mens ionisering refererer til dannelsen af ioner fra et neutralt molekyle.
* Tilstedeværelsen af opløste ioner påvirker vandets egenskaber: Dissociation af ioniske forbindelser fører til dannelsen af elektrolytter, som kan lede elektricitet.
Sig til, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
 Forskerhold dechifrerer enzymatisk nedbrydning af sukker fra marine algerEnzymer er biokatalysatorer, der er afgørende for nedbrydningen af tangbiomasse i havene. For første gang, et internationalt hold af 19 forskere afkodede for nylig den komplette nedbrydningsvej for
Forskerhold dechifrerer enzymatisk nedbrydning af sukker fra marine algerEnzymer er biokatalysatorer, der er afgørende for nedbrydningen af tangbiomasse i havene. For første gang, et internationalt hold af 19 forskere afkodede for nylig den komplette nedbrydningsvej for -
 Indesluttet magnetisk kolloidt system til kontrollerbar væsketransportSkema af indesluttede kolloider i forskellige tilstande via fjern og dynamisk magnetisk regulering Kredit:Science China Press Kolloide suspensioner af mikroskopiske partikler viser kompleks og int
Indesluttet magnetisk kolloidt system til kontrollerbar væsketransportSkema af indesluttede kolloider i forskellige tilstande via fjern og dynamisk magnetisk regulering Kredit:Science China Press Kolloide suspensioner af mikroskopiske partikler viser kompleks og int -
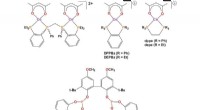 Nyt koboltkompleks kunne reducere omkostningerne ved hydroformyleringStrukturer af cobaltkatalysator-forstadier og biphenphos-ligand i denne undersøgelse. Kredit: Videnskab (2020). DOI:10.1126/science.aaw7742 Et team af forskere fra Louisiana State University og E
Nyt koboltkompleks kunne reducere omkostningerne ved hydroformyleringStrukturer af cobaltkatalysator-forstadier og biphenphos-ligand i denne undersøgelse. Kredit: Videnskab (2020). DOI:10.1126/science.aaw7742 Et team af forskere fra Louisiana State University og E -
 Vil lithium-luft-batterier nogensinde flyve?Kredit:CC0 Public Domain Midt i stigende klimabekymringer, mange regeringer og videnskabsmænd verden over forsøger at reducere flyrejsers miljøpåvirkning. Elektriske fly er en mulig løsning, men d
Vil lithium-luft-batterier nogensinde flyve?Kredit:CC0 Public Domain Midt i stigende klimabekymringer, mange regeringer og videnskabsmænd verden over forsøger at reducere flyrejsers miljøpåvirkning. Elektriske fly er en mulig løsning, men d
- Har gas mere kinetisk energi med højde?
- Hvilken Golf er tættest på nul grader breddegrad og længdegrad?
- Hvilke oplysninger har du brug for at kende til at bestemme den kemiske formel for en ukendt forbind…
- Hvad er navnene på stjerner Hercules -konstellation?
- Ægteskabet mellem topologi og magnetisme i et Weyl -system
- Scavengers of the Tundra


