Fluor Atomic Radius:Sammenligning med Oxygen &Chlorine
* Fluor (F): Den mindste atomradius blandt de tre.
* Oxygen (O): Større end fluor, men mindre end klor.
* Klor (Cl): Den største atomradius af de tre.
Hvorfor er det?
* Periodiske tendenser: Atomradius stiger generelt, når du bevæger dig ned i en gruppe (kolonne) på det periodiske system og falder, når du bevæger dig hen over en periode (række) fra venstre mod højre.
* Elektronegativitet: Fluor er det mest elektronegative element, hvilket betyder, at det stærkt tiltrækker elektroner. Dette stærke træk gør elektronskyen mere kompakt, hvilket resulterer i en mindre atomradius.
* Afskærmning: Når du bevæger dig ned ad en gruppe, øges antallet af elektronskaller, hvilket skaber mere afskærmning mellem kernen og de yderste elektroner. Dette reducerer den effektive nukleare ladning og udvider den atomare radius.
Opsummering:
Fluors lille atomradius skyldes dets høje elektronegativitet og det faktum, at det kun har to elektronskaller. Ilt har en større radius på grund af dets lidt lavere elektronegativitet og en ekstra elektronskal. Klor har den største radius, fordi det har endnu flere elektronskaller, hvilket giver større afskærmning og reducerer den effektive nukleare ladning.
Sidste artikelSalpetersyre vs. Svovlsyre:Forståelse af surhed
Næste artikelIonisk dissociation i vand:En omfattende forklaring
 Varme artikler
Varme artikler
-
 At afsløre træets nanostruktur kan hjælpe med at hæve højdegrænserne for træskyskrabereKredit:CC0 Public Domain Der er stigende interesse rundt om i verden for at bruge træ som lighter, mere bæredygtigt byggealternativ til stål og beton. Mens træ har været brugt i bygninger i årtusi
At afsløre træets nanostruktur kan hjælpe med at hæve højdegrænserne for træskyskrabereKredit:CC0 Public Domain Der er stigende interesse rundt om i verden for at bruge træ som lighter, mere bæredygtigt byggealternativ til stål og beton. Mens træ har været brugt i bygninger i årtusi -
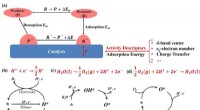 Aktivitetsbeskrivelser for elektrokatalysatorer i energilagringsapplikationer(a) Forskellige aktivitetsdeskriptorer for elektrokemiske reaktioner og katalytiske cyklusser af (b) hydrogenudviklingsreaktion, (c) oxygenudviklingsreaktion og (d) oxygenreduktionsreaktion i brændsel
Aktivitetsbeskrivelser for elektrokatalysatorer i energilagringsapplikationer(a) Forskellige aktivitetsdeskriptorer for elektrokemiske reaktioner og katalytiske cyklusser af (b) hydrogenudviklingsreaktion, (c) oxygenudviklingsreaktion og (d) oxygenreduktionsreaktion i brændsel -
 Unik ferroelektrisk mikrostruktur afsløret for første gangEt atomisk opløst scanningstransmissionselektronmikroskopi (STEM) billede af de polære nanoregioner (PNRer) indlejret i den ikke-polære matrix i det lagdelte perovskitmateriale (Ca, Sr)3Mn2O7. Lys kon
Unik ferroelektrisk mikrostruktur afsløret for første gangEt atomisk opløst scanningstransmissionselektronmikroskopi (STEM) billede af de polære nanoregioner (PNRer) indlejret i den ikke-polære matrix i det lagdelte perovskitmateriale (Ca, Sr)3Mn2O7. Lys kon -
 Tekstilsensorplaster lavet med ledende garn kunne registrere trykpunkter for amputeredeForsker fandt ud af, at en tekstilsensor kan detektere trykpunkter på soklen på en protese. Kredit:North Carolina State University En blød, fleksibelt sensorsystem skabt med elektrisk ledende garn
Tekstilsensorplaster lavet med ledende garn kunne registrere trykpunkter for amputeredeForsker fandt ud af, at en tekstilsensor kan detektere trykpunkter på soklen på en protese. Kredit:North Carolina State University En blød, fleksibelt sensorsystem skabt med elektrisk ledende garn
- Hvilken er den stærkeste base, hvad natriumhydroxid eller kaliumhydroxid?
- Forskere forbedrer det vestlige nordlige Stillehavs tropiske cyklonintensitetsprognoser ved hjælp a…
- Hvad er formen på en Sun Moon -planet eller stjerne?
- Hvad er bevægelsen af et objekt mod Jorden udelukkende fordi tyngdekraften?
- Sådan certificeres en kvantecomputer
- Astronauten og månevandreren Alan Bean dør i en alder af 86


