Salpetersyre vs. Svovlsyre:Forståelse af surhed
Her er hvorfor:
* Syrens styrke: Surhedsgraden bestemmes af en syres evne til at donere protoner (H+ ioner). Svovlsyre er en stærkere syre, fordi den let donerer begge sine protoner, mens salpetersyre kun donerer den ene.
* Elektronegativitet: Svovlatomet i svovlsyre er mere elektronegativt end nitrogenatomet i salpetersyre. Dette betyder, at svovl tiltrækker elektroner stærkere, hvilket fører til en mere polariseret O-H-binding og en større tendens til at frigive protoner.
* Resonansstabilisering: Sulfat-ionen (SO4²⁻) er mere resonansstabiliseret end nitrationen (NO3⁻). Denne stabilisering gør det lettere for svovlsyre at miste sine protoner.
Opsummering: Svovlsyre har en højere tendens til at donere protoner, hvilket gør det til en stærkere syre end salpetersyre.
 Varme artikler
Varme artikler
-
 Nanopartikler i lithium-svovlbatterier opdaget med neutroneksperimentoperandocellen er udviklet hos HZB og gør det muligt at analysere processer inde i batteriet under opladningscyklusser med neutroner. Kredit:S. Risse/HZB Lithium-svovl-batterier betragtes som en a
Nanopartikler i lithium-svovlbatterier opdaget med neutroneksperimentoperandocellen er udviklet hos HZB og gør det muligt at analysere processer inde i batteriet under opladningscyklusser med neutroner. Kredit:S. Risse/HZB Lithium-svovl-batterier betragtes som en a -
 Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe
Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe -
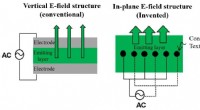 Tekstilfiberindlejret multiluminescerende enhed til fremtidige bærbare enhederStrukturen på eksisterende lysemitterende enhed (venstre) og en ny enhed med elektroder inde i det lysemitterende lag (højre) Kredit:DGIST Dr. Soon Moon Jeongs forskerhold i Division of Energy Tec
Tekstilfiberindlejret multiluminescerende enhed til fremtidige bærbare enhederStrukturen på eksisterende lysemitterende enhed (venstre) og en ny enhed med elektroder inde i det lysemitterende lag (højre) Kredit:DGIST Dr. Soon Moon Jeongs forskerhold i Division of Energy Tec -
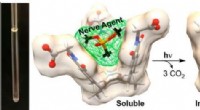 Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.
Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.
- Hvordan genbruger jeg Dewalt 18V batterier?
- Hvad er en styrke, der altid modsætter sig et objekts bevægelse?
- Gennembrud i tynde elektrisk ledende ark baner vej for mindre elektroniske enheder
- Reliance fusionerer musikapps midt i stigningen i streaming i Indien
- Flydende robotter afslører, hvor meget luftbåren støv befrugter det sydlige ocean – en vigtig kli…
- Hvad er et partnerskab mellem organismer, der hjælper en eller begge af dem med at overleve?


