SiO2-binding:kovalent eller ionisk? Forståelse af siliciumdioxid
* Kovalent binding: Silicium og oxygen deler elektroner for at danne bindingerne i SiO2-molekylet. Denne deling af elektroner er den definerende karakteristik af kovalent binding.
* Ikke-polær kovalent: Mens oxygenatomet er mere elektronegativt end siliciumatomet, er elektronegativitetsforskellen ikke stor nok til at skabe en signifikant polaritet i Si-O-bindingerne. Molekylet har en symmetrisk struktur, hvor de to oxygenatomer trækker lige meget på de delte elektroner, hvilket resulterer i et upolært molekyle.
Nøglepunkter:
* Elektronegativitetsforskel: Elektronegativitetsforskellen mellem silicium (1,9) og oxygen (3,44) er 1,54. Denne forskel falder inden for området for polære kovalente bindinger, men den symmetriske struktur af SiO2 resulterer i et samlet ikke-polært molekyle.
* Ionisk binding: I ionbinding er der en fuldstændig overførsel af elektroner fra et atom til et andet, hvilket skaber modsat ladede ioner, der tiltrækker hinanden. Dette sker ikke i SiO2.
Lad mig vide, hvis du vil have flere detaljer om nogen af disse koncepter!
 Varme artikler
Varme artikler
-
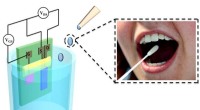 Biologisk sensor kan registrere glukoseniveauer i spyt mere præcist og omkostningseffektivt end blo…Forskere har udviklet en meget følsom, nøjagtig, fleksibel og overkommelig biologisk sensor, der kan registrere glukoseniveauer i spyt. Kredit:Hong Kong Polytechnic University Diabetes er en stofs
Biologisk sensor kan registrere glukoseniveauer i spyt mere præcist og omkostningseffektivt end blo…Forskere har udviklet en meget følsom, nøjagtig, fleksibel og overkommelig biologisk sensor, der kan registrere glukoseniveauer i spyt. Kredit:Hong Kong Polytechnic University Diabetes er en stofs -
 Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange
Fremtidens MOF'er:Konvertering af krystallinske metal-organiske rammer til glas eller væskeKrystallinske MOFer bliver nu omdannet til glas/flydende tilstande, åbne nye applikationer. Kredit:Mindy Takamiya Metal-organiske rammer (MOFer) er porøse, krystallinske materialer, der kan fange -
 Nyt værktøj til at forudsige polymeregenskaberKredit:Gent Universitet Et tværfagligt team af forskere har udviklet et kraftfuldt matematisk modelleringsværktøj, der vil give forskere mulighed for at forudsige egenskaberne af polymernetværk, f
Nyt værktøj til at forudsige polymeregenskaberKredit:Gent Universitet Et tværfagligt team af forskere har udviklet et kraftfuldt matematisk modelleringsværktøj, der vil give forskere mulighed for at forudsige egenskaberne af polymernetværk, f -
 Forskere opnår hidtil uset kontrol over polymergitreKovalente organiske rammer (COFer) tilbyder en unik kombination af egenskaber, der viser lovende for vandrensning, energilagring og elektronisk udstyr. Kredit:Northwestern University Syntetiske po
Forskere opnår hidtil uset kontrol over polymergitreKovalente organiske rammer (COFer) tilbyder en unik kombination af egenskaber, der viser lovende for vandrensning, energilagring og elektronisk udstyr. Kredit:Northwestern University Syntetiske po
- Forbindelse ord for lys kommer fra stjerner?
- 0,125 tommer er hvor mange millimeter?
- Polariseret lys - en enkel vej til meget chirale materialer
- Neutronspektroskopi afslører, at almindelig iltsvampkatalysator også opsuger brint
- Uganda:20 % fald i økonomisk produktion uden klimaindsats
- Hvad er de 12 store tektoniske plader, og hvor de placerede på et globalt kort?


