Entropiændring i forbrændingen af propan:En detaljeret analyse
2 C₃H6(g) + 9 O₂(g) → 6 CO₂(g) + 6 H2O(g)
Forstå entropi
Entropi (S) er et mål for uorden eller tilfældighed i et system. Sådan gælder det for kemiske reaktioner:
* Øget lidelse =Øget entropi: Reaktioner, der producerer flere molekyler eller molekyler med større bevægelsesfrihed (som gasser), har generelt en positiv entropiændring (ΔS> 0).
* Reduceret lidelse =Reduceret entropi: Reaktioner, der resulterer i færre molekyler eller mere begrænset bevægelse (som faste stoffer), har generelt en negativ entropiændring (ΔS <0).
Analyse af reaktionen
* Reaktanter: Vi starter med 2 mol C₃H6 og 9 mol O₂, i alt 11 mol gas.
* Produkter: Vi slutter med 6 mol CO₂ og 6 mol H₂O, i alt 12 mol gas.
Nøgleobservationer:
* Flere mol gas: Antallet af gasmolekyler stiger fra 11 til 12. Dette betyder øget uorden, hvilket fører til en positiv entropiændring.
* Lignende molekylær kompleksitet: Både reaktanter og produkter indeholder relativt simple molekyler. Denne faktor bidrager ikke væsentligt til entropiændringen.
Konklusion
Reaktionen 2 C₃H6(g) + 9 O₂(g) → 6 CO₂(g) + 6 H2O(g) har en positiv entropiændring (ΔS> 0). Dette skyldes primært stigningen i antallet af gasmolekyler.
Vigtig bemærkning: Denne analyse er baseret på generelle tendenser og giver ikke en præcis kvantitativ værdi for entropiændringen. En mere nøjagtig bestemmelse ville kræve anvendelse af standard molære entropiværdier for hver reaktant og produkt.
Sidste artikelCalciumchlorid (CaCl₂):Forståelse af ionisk binding
Næste artikelCurium-elektronkonfiguration:Forståelse af atomstruktur
 Varme artikler
Varme artikler
-
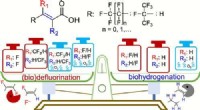 Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning
Under anaerobe forhold kan almindelige mikrobielle samfund bryde den ultra-stærke kulstof-fluor-bin…Kredit:Yaochun Yu et al., Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c05509 Ingeniører ved University of California Riverside er de første til at rapportere selektiv nedbrydning -
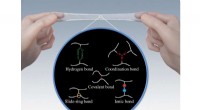 Elastomerer udvikler stærkere bindingsbindingerForskellige former for bindinger kan forbinde elastomerkæder sammen, ændre hvordan materialet opfører sig. Kredit:Yukikazu Takeoka Elastomerer er de bløde, elastiske materialer, som geler og gummi
Elastomerer udvikler stærkere bindingsbindingerForskellige former for bindinger kan forbinde elastomerkæder sammen, ændre hvordan materialet opfører sig. Kredit:Yukikazu Takeoka Elastomerer er de bløde, elastiske materialer, som geler og gummi -
 Hybride enzymkatalysatorer syntetiseret ved en de novo tilgang til udvidelse af biokatalyseKredit:Chinese Journal of Catalysis De to store udfordringer i industriel enzymatisk katalyse er det begrænsede antal kemiske reaktionstyper, der katalyseres af enzymer og ustabilitet af enzymer u
Hybride enzymkatalysatorer syntetiseret ved en de novo tilgang til udvidelse af biokatalyseKredit:Chinese Journal of Catalysis De to store udfordringer i industriel enzymatisk katalyse er det begrænsede antal kemiske reaktionstyper, der katalyseres af enzymer og ustabilitet af enzymer u -
 Ny 3D-trykningsteknik producerer levende 4-D materialerUNSW-forskere har kombineret 3D-print med en lysstyret proces for at skabe en levende 4D-harpiks. Kredit:Shutterstock Reparation og genbrug af plast og levering af kræftmedicin mere effektivt er k
Ny 3D-trykningsteknik producerer levende 4-D materialerUNSW-forskere har kombineret 3D-print med en lysstyret proces for at skabe en levende 4D-harpiks. Kredit:Shutterstock Reparation og genbrug af plast og levering af kræftmedicin mere effektivt er k
- Hvordan påvirker vind og vand geologiske træk?
- Hvad er anvendelsen af ikt i undervisning i biologi.?
- Hvad er den kemiske formel for aluminium og fosfor?
- Hvad er den gåte, der taler om at hente ting, hvor de fleste gætter på, når virkeligheden en mag…
- Plast forgifter havbakterier, der støtter den marine fødekæde
- Hvad er den bedste energikilde for et økosystem?


