Forståelse af polære molekyler:typer, egenskaber og eksempler
1. Vand (H₂O): Vand er det klassiske eksempel på et polært molekyle. Iltatomet er mere elektronegativt end hydrogenatomerne, hvilket betyder, at det tiltrækker elektroner stærkere. Dette skaber en delvis negativ ladning på ilten og delvis positiv ladning på brinterne. Denne ujævne fordeling af ladning gør molekylet polært.
2. Ammoniak (NH3): I lighed med vand er nitrogen i ammoniak mere elektronegativt end brint. Dette skaber en delvis negativ ladning på nitrogenet og delvise positive ladninger på hydrogenerne. Ammoniakmolekylets form med dets enlige elektronpar bidrager også til dets polære natur.
3. Hydrogenchlorid (HCl): I HCl er klor meget mere elektronegativt end brint. Dette resulterer i en stærk delvis negativ ladning på klor og en stærk delvis positiv ladning på brint. Denne betydelige forskel i elektronegativitet gør HCl til et meget polært molekyle.
Vigtig bemærkning: Polaritet opstår fra den ujævne fordeling af elektroner i et molekyle, typisk på grund af forskelle i elektronegativitet mellem atomer. Formen på molekylet spiller også en væsentlig rolle.
 Varme artikler
Varme artikler
-
 Forstå Celsius vs. Fahrenheit-skalaen:Nøgleforskelle og konverteringsvejledningAf Jon Zamboni Opdateret 24. marts 2022 Ridofranz/iStock/GettyImages Fahrenheit- og Celsius-skalaerne er de to mest almindelige temperaturskalaer. Men **de to skalaer bruger forskellige målinger f
Forstå Celsius vs. Fahrenheit-skalaen:Nøgleforskelle og konverteringsvejledningAf Jon Zamboni Opdateret 24. marts 2022 Ridofranz/iStock/GettyImages Fahrenheit- og Celsius-skalaerne er de to mest almindelige temperaturskalaer. Men **de to skalaer bruger forskellige målinger f -
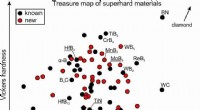 Find alternativer til diamanter til boringDiamant er et af de eneste materialer, der er hårde og seje nok til konstant slibning uden betydelig slid, men diamanter er dyre. Høje omkostninger driver søgen efter nye hårde og superhårde materiale
Find alternativer til diamanter til boringDiamant er et af de eneste materialer, der er hårde og seje nok til konstant slibning uden betydelig slid, men diamanter er dyre. Høje omkostninger driver søgen efter nye hårde og superhårde materiale -
 Persistente vs. ikke-persistente kemikalier:Levetid, toksicitet og miljøpåvirkningKemikalier kommer ind i vores miljø gennem industrielle processer, landbrug og hverdagsprodukter. De kan bredt kategoriseres som vedvarende eller ikke-vedvarende baseret på hvor længe de forbliver i m
Persistente vs. ikke-persistente kemikalier:Levetid, toksicitet og miljøpåvirkningKemikalier kommer ind i vores miljø gennem industrielle processer, landbrug og hverdagsprodukter. De kan bredt kategoriseres som vedvarende eller ikke-vedvarende baseret på hvor længe de forbliver i m -
 Programmerbar dråbe manipulation med en magnetisk aktiverings robotTypisk adfærd for dråberne manipuleret ved hjælp af den magnetisk aktiverede robot. Kredit:Science Advances, doi:10.1126/sciadv.aay5808 Dråbe manipulation i materialevidenskab kan bidrage til vand
Programmerbar dråbe manipulation med en magnetisk aktiverings robotTypisk adfærd for dråberne manipuleret ved hjælp af den magnetisk aktiverede robot. Kredit:Science Advances, doi:10.1126/sciadv.aay5808 Dråbe manipulation i materialevidenskab kan bidrage til vand
- Hvordan tester geologer klipper?
- Hvordan vand driver fotosyntese:Nøglen til plantevækst og jordens ilt
- Fjernforbindelser? Udfiltring af sammenfiltring i kvantefysik
- Hvilken forbindelse dannes, når beryllium og natrium kombineres?
- Hvor mange centimeter svarer til 180 fod?
- Væskedynamikmodel forudsiger nøjagtigt, hvordan bobler påvirker faste overflader


