Dannelse af natrium-klorbinding:Elektronoverførsel forklaret
Det grundlæggende
* Natrium (Na): Har én valenselektron (elektron i dens yderste skal).
* Klor (Cl): Har syv valenselektroner.
Reaktionen
Natrium har en stærk tendens til at miste sin enkeltvalenselektron og bliver til en positivt ladet ion (Na+). Klor har på den anden side en stærk tendens til at få én elektron til at fylde dens yderste skal og bliver til en negativt ladet ion (Cl-).
Når natrium og klor reagerer, overføres natriumatomet dens enkeltvalenselektron til kloratomet. Denne overførsel skaber en elektrostatisk tiltrækning mellem de modsat ladede ioner. Denne attraktion er det, der holder dem sammen i et ionisk bånd .
Resultatet
Den resulterende forbindelse er natriumchlorid (NaCl) , almindeligvis kendt som bordsalt. Det er en neutral forbindelse, fordi den positive ladning af natriumionen (Na+) udligner den negative ladning af chloridionen (Cl-).
Nøglepunkter
* Ionisk binding: Overførsel af elektroner er den definerende karakteristik af ionbinding.
* Elektrostatisk attraktion: Ionernes modsatte ladninger holder dem sammen i en stærk binding.
* Stabil konfiguration: Både natrium og klor opnår en stabil elektronkonfiguration ved at få eller tabe elektroner. Natrium bliver som ædelgassen neon, og klor bliver som ædelgassen argon.
 Varme artikler
Varme artikler
-
 Syntese af et sjældent metalkompleks af dinitrogenoxid åbner nye udsigter forKredit:Monika Stolar og Chris Gendy Ligesom dets kemiske relative kuldioxid (CO 2 ), dinitrogenoxid (N 2 O) er en vigtig drivhusgas og det dominerende ozonnedbrydende stof, der udsendes i det
Syntese af et sjældent metalkompleks af dinitrogenoxid åbner nye udsigter forKredit:Monika Stolar og Chris Gendy Ligesom dets kemiske relative kuldioxid (CO 2 ), dinitrogenoxid (N 2 O) er en vigtig drivhusgas og det dominerende ozonnedbrydende stof, der udsendes i det -
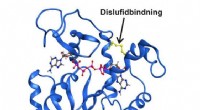 At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers
At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers -
 Blyfri magnetiske perovskitterKredit:CC0 Public Domain Forskere ved Linköpings Universitet, Sverige, arbejder med perovskite-materialefamilien, har udviklet en optoelektronisk magnetisk dobbeltperovskit. Opdagelsen åbner mulig
Blyfri magnetiske perovskitterKredit:CC0 Public Domain Forskere ved Linköpings Universitet, Sverige, arbejder med perovskite-materialefamilien, har udviklet en optoelektronisk magnetisk dobbeltperovskit. Opdagelsen åbner mulig -
 Potentielle antimikrobielle fundet, der viser løfte om bekæmpelse af stafylokokinfektionerEric Brown (til venstre), professor i biokemi og biomedicinsk videnskab, og Omar El-Halfawy, en postdoc i biokemi og biomedicinske videnskaber, ved McMaster University. Kredit:McMaster University
Potentielle antimikrobielle fundet, der viser løfte om bekæmpelse af stafylokokinfektionerEric Brown (til venstre), professor i biokemi og biomedicinsk videnskab, og Omar El-Halfawy, en postdoc i biokemi og biomedicinske videnskaber, ved McMaster University. Kredit:McMaster University
- Forståelse af kulilte:sammensætning og formel
- Hvordan trodser morfisk fysik?
- Hvorfor falder alle genstande til jorden med samme hastighed, selvom acceleration på grund af tyngd…
- Hvilken forbindelse dannes som en almindelig del af processen fotosyntesen?
- Hvad er seismiske bølger, og hvornår dannes de?
- Et overraskende eksperiment åbner vejen til nye partikelmanipulationsmetoder


