Metal-ikke-metal binding:Ionisk vs. kovalent - Forståelse af kemiske reaktioner
Her er hvorfor:
* Metalbindinger: Metaller binder sig til andre metaller gennem et "hav af elektroner", hvor elektroner delokaliseres og deles i hele strukturen.
* ioniske bindinger: Metaller reagerer med ikke-metaller og danner ionbindinger. Ved ionbinding mister metalatomet elektroner for at blive en positivt ladet kation, og ikke-metalatomet får elektroner til at blive en negativt ladet anion. Disse modsat ladede ioner tiltrækker hinanden elektrostatisk.
Kovalente bindinger involverer deling af elektroner mellem to ikke-metalatomer.
Opsummering: Når et metal reagerer med et ikke-metal, en ionisk binding er dannet, ikke en kovalent binding.
 Varme artikler
Varme artikler
-
 Forskere udnytter gelpolymerelektrolyt til højtydende magnesiumbatterierDet skematiske diagram over strukturen og anvendelsesområderne for PTB@GF-GPE Kredit:DU Aobing Elektroniske produkter, elektriske køretøjer og storstilet energilagring, der er tæt knyttet til menn
Forskere udnytter gelpolymerelektrolyt til højtydende magnesiumbatterierDet skematiske diagram over strukturen og anvendelsesområderne for PTB@GF-GPE Kredit:DU Aobing Elektroniske produkter, elektriske køretøjer og storstilet energilagring, der er tæt knyttet til menn -
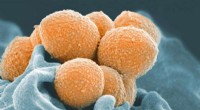 Sukker fra modermælk kan hjælpe med at behandle, forebygge infektioner hos nyfødteEt scanningselektronmikroskopbillede af gruppe A Streptococcus (orange) under fagocytisk interaktion med en human neutrofil (blå). Kredit:NIAID Bakterier kendt som gruppe B Streptococcus (GBS) er
Sukker fra modermælk kan hjælpe med at behandle, forebygge infektioner hos nyfødteEt scanningselektronmikroskopbillede af gruppe A Streptococcus (orange) under fagocytisk interaktion med en human neutrofil (blå). Kredit:NIAID Bakterier kendt som gruppe B Streptococcus (GBS) er -
 Et strejf salt kan styrke MXene -supermaterialer mod oxidationVed at kombinere et almindeligt føde- og vandadditiv, pholyphosphatsalte, med MXene materialer, forskere på Drexel har opdaget en måde at bremse oxidationsprocessen på, når de udsættes for vand. Kredi
Et strejf salt kan styrke MXene -supermaterialer mod oxidationVed at kombinere et almindeligt føde- og vandadditiv, pholyphosphatsalte, med MXene materialer, forskere på Drexel har opdaget en måde at bremse oxidationsprocessen på, når de udsættes for vand. Kredi -
 Mikrobølger mod koldstart-emissionerDen geometriske keramiske struktur af testkatalysatoren designet på computeren. Specialister hos Empa coated det med det katalytisk aktive lag og testede renseeffekten i en kunstig strøm af udstødning
Mikrobølger mod koldstart-emissionerDen geometriske keramiske struktur af testkatalysatoren designet på computeren. Specialister hos Empa coated det med det katalytisk aktive lag og testede renseeffekten i en kunstig strøm af udstødning
- Er N et grundstof eller en forbindelse?
- Kunstig intelligens bot uddannet til at genkende galakser
- Sådan rydder du op i rumaffald - ved hjælp af spilteori
- Mængde kinetisk og potentiel energi et objekt?
- Et hårdt kig på polymerer i cementblanding
- Hvad er processen med molekyler, der bryder sammen i tarmen?


