At forstå atomemission:Hvordan atomer producerer lys
1. Elektroner og energiniveauer:
* Atomstruktur: Atomer består af en kerne (protoner og neutroner) omgivet af elektroner, der kredser i bestemte energiniveauer kaldet elektronskaller.
* Grundtilstand: Elektroner optager normalt de lavest mulige energiniveauer, en tilstand kendt som grundtilstanden.
2. Energiabsorbering:
* Excitation: Når et atom absorberer energi (f.eks. fra varme, elektricitet eller lys), kan en elektron hoppe til et højere energiniveau. Dette kaldes excitation.
* Typer af excitation:
* Varme: Den termiske bevægelse af atomer kan forårsage kollisioner, der exciterer elektroner.
* Lys: Fotoner (pakker af lysenergi) kan absorberes af elektroner, hvilket får dem til at hoppe energiniveauer.
3. Energifrigivelse:Emission af lys
* Ophidset tilstand: Den exciterede elektron er ustabil og ønsker at vende tilbage til sit lavere energiniveau.
* Fotoemission: For at vende tilbage til grundtilstanden frigiver elektronen den overskydende energi som en foton af lys.
* Farve og energi: Farven på det udsendte lys afhænger af energiforskellen mellem den exciterede tilstand og grundtilstanden. Højere energiforskelle resulterer i højere frekvens (blåere) lys.
4. Kvantespring:
* Diskrete energiniveauer: Elektroner kan kun eksistere ved specifikke energiniveauer, ikke midt imellem. Dette er et grundlæggende princip i kvantemekanikken.
* Energikvanta: Energiforskellen mellem to energiniveauer er en diskret mængde kaldet et "kvantum" af energi.
* Fotoemission: Når en elektron falder til et lavere energiniveau, udsender den en foton med præcis energiforskellen mellem de to niveauer.
Eksempel:
* Forestil dig en stige med trin, der repræsenterer energiniveauer. En elektron, der klatrer op ad et trin, absorberer energi, og når den falder ned igen, udsender den en foton af lys, der svarer til energiforskellen mellem trinene.
Nøglepunkter:
* Lysemission fra atomer er en kvanteproces.
* Lysets farve bestemmes af energiforskellen mellem elektronenerginiveauer.
* Forskellige atomer har forskellige energiniveaustrukturer, hvilket fører til unikke emissionsspektre.
Applikationer:
* Spektroskopi: Forskere analyserer det lys, der udsendes af atomer, for at identificere grundstoffer og studere deres egenskaber.
* Pærer: Glødepærer bruger varme til at excitere elektroner i en glødetråd, hvilket får den til at gløde.
* Lasere: Lasere bruger stimuleret emission til at forstærke lyset og producerer stærkt fokuserede stråler.
 Varme artikler
Varme artikler
-
 Innovative carbon nanorør fotokatalytiske materialer til effektiv omdannelse af solenergi og brintp…Figur 1:Absorptionsspektrum af s-SWCNTer (sort linje) overlejret med solspektrum (gul linje). Kredit:Okayama University De unikke egenskaber ved halvledende enkeltvæggede carbon-nanorør (s-SWCNTer
Innovative carbon nanorør fotokatalytiske materialer til effektiv omdannelse af solenergi og brintp…Figur 1:Absorptionsspektrum af s-SWCNTer (sort linje) overlejret med solspektrum (gul linje). Kredit:Okayama University De unikke egenskaber ved halvledende enkeltvæggede carbon-nanorør (s-SWCNTer -
 Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele
Strækbare og klemme bløde sensorer et skridt nærmere takket være den nye bindingsmetodeEn sensor holdt mellem to fingre. Kredit:Michael Kasimatis Bioingeniører fra Imperial College London har fundet en måde at skabe elastiske og squeezy bløde sensorenheder ved at binde gummi til ele -
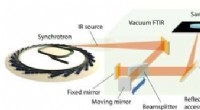 Undersøgelse af de komplekse dielektriske egenskaber af metal-organiske rammer (MOF'er)Figur 1:Den eksperimentelle opsætning til måling af bredbånds-IR-reflektiviteten af polykrystallinske MOF-pellets. De opnåede højopløsningsreflektivitetsdata blev efterfølgende brugt til at bestemme
Undersøgelse af de komplekse dielektriske egenskaber af metal-organiske rammer (MOF'er)Figur 1:Den eksperimentelle opsætning til måling af bredbånds-IR-reflektiviteten af polykrystallinske MOF-pellets. De opnåede højopløsningsreflektivitetsdata blev efterfølgende brugt til at bestemme -
 Energihøstende plastik består syretestenDiego Rosas-Villalva forklarede, at holdet var overrasket over, at en så ekstremt tynd polymer var så effektiv til at forbedre enhedens levetid. Kredit:KAUST En polymer, der tidligere blev brugt t
Energihøstende plastik består syretestenDiego Rosas-Villalva forklarede, at holdet var overrasket over, at en så ekstremt tynd polymer var så effektiv til at forbedre enhedens levetid. Kredit:KAUST En polymer, der tidligere blev brugt t
- Hvorfor er planter nyttige i en eg skov?
- Om Rutherfords Guldfolie Eksperiment
- Hvad dækker Savannahs i Afrika?
- Ny undersøgelse viser, hvor hurtigt overfladevand bevæger sig til grundvandsreservoirer i hele Aus…
- Ny enzymnøgle til bedre behandling af Parkinsons sygdom
- Gør 3D-printning smartere med maskinlæring


