Forståelse af de fysiske tilstande af kovalente forbindelser
Kovalente forbindelser dannes ved deling af elektroner mellem atomer. Tilstanden af en kovalent forbindelse (fast, flydende eller gas) afhænger af flere faktorer, herunder:
* Strength of intermolecular forces: Disse kræfter er tiltrækningen mellem molekyler. Stærkere intermolekylære kræfter fører til et højere smelte- og kogepunkt, hvilket gør forbindelsen mere tilbøjelig til at være fast ved stuetemperatur.
* Molekylær størrelse og form: Større molekyler og mere komplekse former har generelt stærkere intermolekylære kræfter.
* Polaritet: Polære molekyler (med ujævn fordeling af elektrontæthed) har stærkere dipol-dipol-kræfter, som kan føre til en flydende eller fast tilstand ved stuetemperatur.
Her er nogle generelle tendenser:
* Gasser: Små, ikke-polære kovalente molekyler som metan (CH4) og kuldioxid (CO2) er gasser ved stuetemperatur.
* Væsker: Mange kovalente forbindelser med moderate intermolekylære kræfter er væsker ved stuetemperatur, såsom vand (H2O) og ethanol (C2H5OH).
* Faststoffer: Kovalente forbindelser med store molekyler, stærke intermolekylære kræfter eller netværksstrukturer (som diamanter eller siliciumdioxid) har en tendens til at være faste stoffer ved stuetemperatur.
Det er vigtigt at huske: Der er undtagelser fra disse generelle tendenser, og tilstanden af en bestemt kovalent forbindelse kan variere afhængigt af de specifikke forhold (temperatur og tryk).
Lad mig vide, hvis du vil have flere detaljer om en specifik kovalent forbindelse!
 Varme artikler
Varme artikler
-
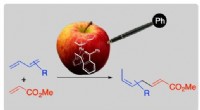 Phenyltilsætning gjorde en gift nyttig til en kemisk reaktion i katalyseTag for eksempel et forgiftet æble, det kan udsende en berusende blød aroma bare ved at stikke en kuglepen og skifte til at være lækker. Kreditering:Figur tilpasset med tilladelse fra Organometallics,
Phenyltilsætning gjorde en gift nyttig til en kemisk reaktion i katalyseTag for eksempel et forgiftet æble, det kan udsende en berusende blød aroma bare ved at stikke en kuglepen og skifte til at være lækker. Kreditering:Figur tilpasset med tilladelse fra Organometallics, -
 Retsmedicinsk kemiker foreslår svedteststrimmel som erstatning for alkometerUniversitetet i Albany retsmedicinsk kemiker Jan Halámek. Kredit:Paul Miller Retsmedicineren Jan Halámek har igen fundet en innovativ anvendelse til menneskelig sved - denne gang for at holde fuld
Retsmedicinsk kemiker foreslår svedteststrimmel som erstatning for alkometerUniversitetet i Albany retsmedicinsk kemiker Jan Halámek. Kredit:Paul Miller Retsmedicineren Jan Halámek har igen fundet en innovativ anvendelse til menneskelig sved - denne gang for at holde fuld -
 Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk
Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk -
 Salt tager et hurtigt skridt, før det falder ud af vandetI et fund med konsekvenser for emner, herunder klimamodeller og lægemiddelproduktion, beregningsmæssig forskning fra Princeton University har beskrevet et yderligere trin i udfældningen af saltkryst
Salt tager et hurtigt skridt, før det falder ud af vandetI et fund med konsekvenser for emner, herunder klimamodeller og lægemiddelproduktion, beregningsmæssig forskning fra Princeton University har beskrevet et yderligere trin i udfældningen af saltkryst


