Kovalente forbindelser ved stuetemperatur:Fysiske tilstande forklaret
* Styrken af de kovalente bindinger: Stærkere bindinger fører til højere smelte- og kogepunkter.
* Molekylets størrelse og form: Større molekyler har mere overfladeareal til intermolekylære kræfter, hvilket fører til højere smelte- og kogepunkter.
* Molekylets polaritet: Polære molekyler har stærkere intermolekylære kræfter end ikke-polære molekyler, hvilket fører til højere smelte- og kogepunkter.
Generelle tendenser:
* Gasser: Kovalente forbindelser med meget svage intermolekylære kræfter er typisk gasser ved stuetemperatur. Eksempler omfatter metan (CH4), kuldioxid (CO2) og nitrogen (N2).
* Væsker: Kovalente forbindelser med moderate intermolekylære kræfter er typisk væsker ved stuetemperatur. Eksempler inkluderer vand (H2O), ethanol (C2H5OH) og acetone (CH3COCH3).
* Fast: Kovalente forbindelser med stærke intermolekylære kræfter er typisk faste stoffer ved stuetemperatur. Eksempler omfatter sukker (C12H22O11), diamant (C) og siliciumdioxid (SiO2).
Undtagelser:
* Netværksbestandigheder: Nogle kovalente forbindelser danner gigantiske strukturer med stærke kovalente bindinger gennem hele strukturen. Disse er typisk meget hårde og har meget høje smeltepunkter, såsom diamant og siliciumcarbid.
* Små, meget polære molekyler: Nogle små, meget polære kovalente molekyler kan have stærke intermolekylære kræfter, hvilket fører til højere smelte- og kogepunkter. Eksempler omfatter vand (H2O) og hydrogenfluorid (HF).
Som konklusion:
Selvom der ikke er nogen enkelt "sædvanlig tilstand" for kovalente forbindelser ved stuetemperatur, vil størstedelen af dem være enten gasser, væsker eller faste stoffer afhængig af ovennævnte faktorer.
Sidste artikelIltgas (O2):Egenskaber og identifikation
Næste artikelForståelse af de fysiske tilstande af kovalente forbindelser
 Varme artikler
Varme artikler
-
 I betragtning af virkningen af den indendørs kemi -cocktailKredit:CC0 Public Domain Et par forskere, et med det kinesiske videnskabsakademi i Kina, den anden med University of Toronto i Canada har genbesøgt emnet indendørs kemi og dens indvirkning på menn
I betragtning af virkningen af den indendørs kemi -cocktailKredit:CC0 Public Domain Et par forskere, et med det kinesiske videnskabsakademi i Kina, den anden med University of Toronto i Canada har genbesøgt emnet indendørs kemi og dens indvirkning på menn -
 Forskere udvikler nye, lavprisværktøj til påvisning af bakterier i mad og vandKredit:University of Massachusetts Amherst Fødevareforsker Lili He og kolleger ved University of Massachusetts Amherst rapporterer, at de har udviklet en ny, hurtig og billig metode til påvisning
Forskere udvikler nye, lavprisværktøj til påvisning af bakterier i mad og vandKredit:University of Massachusetts Amherst Fødevareforsker Lili He og kolleger ved University of Massachusetts Amherst rapporterer, at de har udviklet en ny, hurtig og billig metode til påvisning -
 Kvantearmeringsjern:Kvanteprikker forbedrer stabiliteten af solfangende perovskitkrystallerMengxia Liu er hovedforfatter på et nyt papir i Nature, der beskriver en måde at kombinere to lovende solteknologier - perovskiter og kvanteprikker - for at forbedre deres stabilitet. Kredit:Sanyang H
Kvantearmeringsjern:Kvanteprikker forbedrer stabiliteten af solfangende perovskitkrystallerMengxia Liu er hovedforfatter på et nyt papir i Nature, der beskriver en måde at kombinere to lovende solteknologier - perovskiter og kvanteprikker - for at forbedre deres stabilitet. Kredit:Sanyang H -
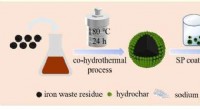 Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
Forskere bruger tobaksaffaldsvæske og jernrester til fjernelse af Cd(II)Skematisk diagram af fremstillingsprocessen og adsorptionsmekanismerne for OWIR@TWL@SP. Kredit:WU Qingchuan Ifølge en ny undersøgelse offentliggjort i Langmuir , blev en slags jernbaseret kulstofmi
- Rapport:Ægteskab af samme køn har ikke forårsaget nogen skade på par af forskellig køn
- Spam, spam overalt -- Hvordan kan vi kontrollere det?
- Navn 5 Igneous Rocks Og hvordan genkender de dem?
- Blev den 21. december -formørkelse forudsagt af mayaer?
- Er det let at få energi fra et lys?
- Hvad er skalaernes funktion på krybdyr?


