Forståelse af kovalente bindinger:fysisk tilstand og molekylære egenskaber
* Kovalente bindinger er de kræfter, der holder atomer sammen i et molekyle. De er ikke et stof i sig selv med en fysisk tilstand.
* Den fysiske tilstand af et stof (fast, flydende eller gas) bestemmes af de intermolekylære kræfter mellem molekyler. Disse kræfter er svagere end kovalente bindinger.
* Typen af kovalent binding kan påvirke stoffets fysiske tilstand. For eksempel kan et molekyle med stærke kovalente bindinger være et fast stof ved stuetemperatur, mens et molekyle med svagere kovalente bindinger kan være en væske eller gas.
Her er et eksempel:
* Vand (H2O) har kovalente bindinger mellem hydrogen- og oxygenatomer.
* Vandmolekylerne selv tiltrækkes af hinanden af hydrogenbinding (en type intermolekylær kraft).
* Denne attraktion er stærk nok til at holde vand i flydende tilstand ved stuetemperatur.
Opsummering:
* Du kan ikke tale om den fysiske tilstand af en kovalent binding.
* Den fysiske tilstand af et stof med kovalente bindinger afhænger af de intermolekylære kræfter mellem molekylerne.
Sidste artikelOxygens oxidationsnummer:Forståelse af reglen og undtagelserne
Næste artikelIltgas (O2):Egenskaber og identifikation
 Varme artikler
Varme artikler
-
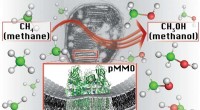 Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University
Metanforbrugende bakterier kan være fremtiden for brændstofDet primære metaboliske enzym i metanotrofe bakterier, partikelformig methanmonooxygenase (pMMO), katalyserer metan-til-methanol-omdannelsen på et sted med en kobberion. Kredit:Northwestern University -
 Nyt brændselscellekoncept bringer biologisk design til bedre elproduktionKredit:CC0 Public Domain Brændselsceller har længe været betragtet som en lovende strømkilde. Disse enheder, opfundet i 1830erne, generere elektricitet direkte fra kemikalier, såsom brint og ilt,
Nyt brændselscellekoncept bringer biologisk design til bedre elproduktionKredit:CC0 Public Domain Brændselsceller har længe været betragtet som en lovende strømkilde. Disse enheder, opfundet i 1830erne, generere elektricitet direkte fra kemikalier, såsom brint og ilt, -
 Er dit maskinlæringstræningssæt forudindtaget? Hvordan man udvikler nye lægemidler baseret på f…Forfatterne kombinerede proprietære (GSK) og publicerede (CCDC) datasæt for bedre at træne maskinlæringsmodeller (ML) til lægemiddelopdagelse. Kredit:Alex Moldovan. Polymorfer er molekyler, der ha
Er dit maskinlæringstræningssæt forudindtaget? Hvordan man udvikler nye lægemidler baseret på f…Forfatterne kombinerede proprietære (GSK) og publicerede (CCDC) datasæt for bedre at træne maskinlæringsmodeller (ML) til lægemiddelopdagelse. Kredit:Alex Moldovan. Polymorfer er molekyler, der ha -
 Peptid-fingeraftryk muliggør tidligere diagnosticering af Alzheimers sygdomNeurale netværk kan detektere små forskelle i farvemønstrene fra tørrede peptidopløsninger (venstre:amyloid beta (Aβ42) peptid; højre:mutation). Kredit:Karlsruhe Institute of Technology Neurodegene
Peptid-fingeraftryk muliggør tidligere diagnosticering af Alzheimers sygdomNeurale netværk kan detektere små forskelle i farvemønstrene fra tørrede peptidopløsninger (venstre:amyloid beta (Aβ42) peptid; højre:mutation). Kredit:Karlsruhe Institute of Technology Neurodegene
- Hvad kaldes også første fjerdedel og tredje måne?
- Hvilken flod har skåret den dybeste i skorpe?
- Hvilken sæson er det, når jordens nordlige halvkugle vippes mod solen?
- De største bio- og abiotiske komponenter i økosystemet i Great Barrier Reef
- Hvordan ved forskere, hvad solen er lavet af i atmosfæren?
- Blodagar og chokolade er typer af berigede medier, der hæmmer bestemt?


