Ksp og ionprodukt:Bestemmelse af opløsningsmætning
Ksp:Mætningspunktet
* Ksp er en specifik ligevægtskonstant, der gælder for opløsning af tungtopløselige ionforbindelser. Det repræsenterer det maksimale produkt af ionkoncentrationer, der kan eksistere i en opløsning ved en given temperatur, før der sker nedbør.
Produktet af ionkoncentrationer (Q)
* Q er ionproduktet og repræsenterer det faktiske produkt af ionkoncentrationer i en opløsning på et givet tidspunkt. Det beregnes ved hjælp af de aktuelle koncentrationer af ionerne i opløsningen.
Forholdet
1. Q
2. Q =Ksp: Løsningen er mættet . Det betyder, at opløsningen er i ligevægt, og ikke mere af ionforbindelsen kan opløses.
3. Q> Ksp: Løsningen er overmættet . Det betyder, at opløsningen indeholder flere opløste ioner, end den kan holde ved ligevægt. Der vil forekomme nedbør for at reducere ionkoncentrationerne tilbage til mætningspunktet (Ksp).
Eksempel
Overvej opløsningen af sølvchlorid (AgCl):
AgCl(s) ⇌ Ag+(aq) + Cl-(aq)
Ksp =[Ag+][Cl-]
* Hvis [Ag+][Cl-]
* Hvis [Ag+][Cl-]> Ksp, er opløsningen overmættet, og AgCl vil fælde ud af opløsningen, indtil produktet af ionkoncentrationer er lig med Ksp.
Opsummering:
Ksp er en konstant, der repræsenterer det maksimale produkt af ionkoncentrationer, der er mulige ved ligevægt. Ved at sammenligne ionproduktet (Q) med Ksp, kan du bestemme, om en opløsning er umættet, mættet eller overmættet, hvilket giver dig mulighed for at forudsige, om der vil forekomme nedbør.
Sidste artikelCarbonoxidationstilstand i isocyanid:En detaljeret forklaring
Næste artikelSaltfarver og glans:Beyond White og Metallic
 Varme artikler
Varme artikler
-
 Diagnostisk platform kunne strække sig til at påvise biomarkører for sygdomZehra Parlak ser på sin proof-of-principle point-of-care diagnostiske enhed, grundlaget for hendes startup-firma kaldet Qatch. Kredit:Duke University Et startup-firma baseret på teknologi licenser
Diagnostisk platform kunne strække sig til at påvise biomarkører for sygdomZehra Parlak ser på sin proof-of-principle point-of-care diagnostiske enhed, grundlaget for hendes startup-firma kaldet Qatch. Kredit:Duke University Et startup-firma baseret på teknologi licenser -
 Frostvæske fisk inspirerer til nye kryobeskyttelsesmidler til menneskelige celler og vævKredit:Horizon:The EU Research &Innovation Magazine Ideen om kryogenisk at fryse en person for at bevare deres krop indtil mange år ud i fremtiden har længe været en fast bestanddel af science fic
Frostvæske fisk inspirerer til nye kryobeskyttelsesmidler til menneskelige celler og vævKredit:Horizon:The EU Research &Innovation Magazine Ideen om kryogenisk at fryse en person for at bevare deres krop indtil mange år ud i fremtiden har længe været en fast bestanddel af science fic -
 Første af sin art hydrogel-platform muliggør on-demand produktion af medicin, kemikalierEt 3D-printet hydrogelgitter indeholder gærceller, der kan muliggøre kontinuerlig produktion af ethanol. Kredit:Cockrell School of Engineering, University of Texas i Austin Et team af kemiske inge
Første af sin art hydrogel-platform muliggør on-demand produktion af medicin, kemikalierEt 3D-printet hydrogelgitter indeholder gærceller, der kan muliggøre kontinuerlig produktion af ethanol. Kredit:Cockrell School of Engineering, University of Texas i Austin Et team af kemiske inge -
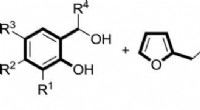 Russiske kemikere udviklede en måde at syntetisere stoffer fra vedvarende prækursorerDen nye enkle syntetiske vej til at opnå benzofuraner fra salicylalkoholer og N-tosylfurfurylamin. Kredit:Igor Trushkov Forskere fra RUDN University og deres russiske kolleger har udviklet en ny t
Russiske kemikere udviklede en måde at syntetisere stoffer fra vedvarende prækursorerDen nye enkle syntetiske vej til at opnå benzofuraner fra salicylalkoholer og N-tosylfurfurylamin. Kredit:Igor Trushkov Forskere fra RUDN University og deres russiske kolleger har udviklet en ny t
- Hvordan kan det at leve i Sahel være forskellig fra en regnskov?
- Blive eller gå? Nogle byer ser på tilbagetog fra havet
- Hvad er atomnummeret og massen af kulstof?
- Hvordan evolutionen har optimeret den magnetiske sensor i fugle
- CSIRO kortlægger Darwins hot spots og varme-sundhedssårbarhed
- Hvad er eksempler på gode ledere (apparater)?


