Lewis-strukturen af svovlfluorid (SF4):En trin-for-trin guide
1. Tæl valenselektronerne: Svovl har 6 valenselektroner, og hver fluor har 7, i alt 6 + (6 x 7) =48 valenselektroner.
2. Placer det mindst elektronegative element i midten: Svovl er mindre elektronegativt end fluor, så det går i midten.
3. Forbind de ydre atomer med enkeltbindinger: Forbind hver fluor til svovlen med en enkeltbinding. Dette bruger op til 12 elektroner (6 bindinger x 2 elektroner pr. binding).
4. Fuldfør oktetterne af de ydre atomer: Hvert fluor har brug for 6 elektroner mere for at fuldende sin oktet. Fordel de resterende 36 elektroner (48 - 12) som enlige par rundt om fluoratomerne.
Den endelige Lewis-struktur ser således ud:
F
|
F - S - F
|
F
|
F
|
F
Vigtige bemærkninger:
* Det centrale svovlatom har 12 elektroner omkring sig, hvilket er mere end en oktet. Dette er tilladt for elementer i den tredje periode og derefter, fordi de kan rumme udvidede oktetter.
* Svovlhexafluorid er et meget stabilt molekyle på grund af de stærke S-F-bindinger og det symmetriske arrangement af fluoratomerne.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Ny biokatalytisk membran fjerner mikroforurenende stoffer på en effektiv og stabil mådeBiokatalytisk membrankonstruktionshypotese inspireret af den flydende mosaikmodel af cellemembranstrukturen. Kredit:ZHANG Hao Mikroforurenende stoffer såsom hormonforstyrrende stoffer, pesticider
Ny biokatalytisk membran fjerner mikroforurenende stoffer på en effektiv og stabil mådeBiokatalytisk membrankonstruktionshypotese inspireret af den flydende mosaikmodel af cellemembranstrukturen. Kredit:ZHANG Hao Mikroforurenende stoffer såsom hormonforstyrrende stoffer, pesticider -
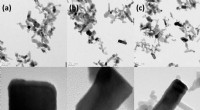 Ingeniører finder en smart måde at omdanne affaldskuldioxid til nyttigt materialeHR-TEM billeder for (a) ZnO-5, (b) ZnO-7 og (c) ZnO-9. Kredit: Avancerede energimaterialer (2020). DOI:10.1002/aenm.202001381 Kemiske ingeniører fra UNSW Sydney har udviklet ny teknologi, der hjæ
Ingeniører finder en smart måde at omdanne affaldskuldioxid til nyttigt materialeHR-TEM billeder for (a) ZnO-5, (b) ZnO-7 og (c) ZnO-9. Kredit: Avancerede energimaterialer (2020). DOI:10.1002/aenm.202001381 Kemiske ingeniører fra UNSW Sydney har udviklet ny teknologi, der hjæ -
 Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit
Ingeniører opdager en ny rolle for vand i produktionen af vedvarende brændstofferOU-ingeniører har opdaget en ny tilgang til vandstøttet opgradering af det vedvarende kemikalie, furfural, fordoble eller tredoble konverteringshastigheden. Kredit:University of Oklahoma Universit -
 Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love
Forskere rekrutterer nye atomare sværvægtere i målrettet kamp mod kræftKatherine Shield (fra venstre), Dahlia An, Tyler Bailey på Lawrence Berkeley National Laboratory tirsdag, 17. november kl. 2020, i Berkeley, Californien Kredit:Marilyn Sargent/Berkeley Lab En love


