Ioniske bindinger:egenskaber, dannelse og karakteristika
Ionbindingers egenskaber:
Ionbindinger er en type kemisk binding dannet af den elektrostatiske tiltrækning mellem modsat ladede ioner . Her er nogle nøgleegenskaber:
1. Dannelse:
* Elektronoverførsel: Ionbindinger dannes, når et atom donerer en elektron (der danner en positivt ladet kation) til et andet atom, der accepterer elektronen (danner en negativt ladet anion).
* Elektrostatisk tiltrækning: De modsatte ladninger af kationen og anionen tiltrækker hinanden og danner en stærk elektrostatisk kraft, der holder ionerne sammen.
2. Styrke:
* Høj styrke: Ionbindinger er generelt meget stærke på grund af den stærke elektrostatiske tiltrækning mellem modsat ladede ioner.
* Smelte- og kogepunkter: Denne styrke fører til høje smelte- og kogepunkter for ioniske forbindelser.
* Opløselighed: Ioniske forbindelser er ofte opløselige i polære opløsningsmidler som vand, da vandmolekylerne kan interagere med de ladede ioner og trække dem fra hinanden.
3. Fysiske egenskaber:
* Krystallinsk struktur: Ioniske forbindelser danner normalt krystaller med et regelmæssigt, gentagne arrangement af ioner.
* Hård og skør: Ioniske forbindelser er typisk hårde og skørt . Når de rammes, kan ionerne skifte, forstyrre den elektrostatiske balance og få krystallen til at bryde.
* Elektrisk ledningsevne: I solid state , ioniske forbindelser er dårlige ledere af elektricitet, fordi ionerne er fikseret på plads. De er dog gode dirigenter når de er smeltet eller opløst i vand, da ionerne kan bevæge sig frit og føre en elektrisk strøm.
4. Andre egenskaber:
* Ikke-retningsbestemt: I modsætning til kovalente bindinger er ionbindinger ikke-retningsbestemte . Den elektrostatiske tiltrækning virker i alle retninger.
* Høj formationsentalpi: Ioniske forbindelser har typisk en høj dannelsesentalpi, hvilket indikerer en stor mængde energi frigivet, når bindingen dannes.
Eksempler på ioniske forbindelser:
* Natriumchlorid (NaCl)
* Calciumfluorid (CaF₂)
* Magnesiumoxid (MgO)
* Kaliumbromid (KBr)
Det er vigtigt at bemærke, at styrken og andre egenskaber ved ionbindinger kan variere afhængigt af de specifikke involverede elementer og deres elektronegativitetsforskel. Imidlertid er de generelle karakteristika beskrevet ovenfor fælles for de fleste ioniske forbindelser.
 Varme artikler
Varme artikler
-
 Mestring af kunsten at afbalancere kemiske ligninger:En praktisk vejledningAf Riti Gupta | Opdateret 30. august 2022 Kamil Macniak/iStock/Getty Images En kemisk reaktion opstår, når et eller flere molekyler omdannes til nye arter. Kemikere repræsenterer disse transformati
Mestring af kunsten at afbalancere kemiske ligninger:En praktisk vejledningAf Riti Gupta | Opdateret 30. august 2022 Kamil Macniak/iStock/Getty Images En kemisk reaktion opstår, når et eller flere molekyler omdannes til nye arter. Kemikere repræsenterer disse transformati -
 Nye materialer hjælper med at udvide volumetrisk 3-D-printVed hjælp af en tilpasset volumetrisk additiv fremstilling 3D-printer, Lawrence Livermore-forskere var i stand til at bygge hårde og stærke, samt strækbar og fleksibel, genstande næsten øjeblikkeligt
Nye materialer hjælper med at udvide volumetrisk 3-D-printVed hjælp af en tilpasset volumetrisk additiv fremstilling 3D-printer, Lawrence Livermore-forskere var i stand til at bygge hårde og stærke, samt strækbar og fleksibel, genstande næsten øjeblikkeligt -
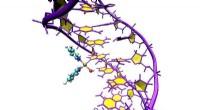 Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi
Hvordan interagerer metaller med DNA?Computersimuleringer viser den præcise placering af Pt103 i DNA. Kredit:Juan J. Nogueira, Universitetet i Wien I et par årtier, metalholdige lægemidler er med succes blevet brugt til at bekæmpe vi -
 Gennemsigtigt træ:fremtidens byggemateriale?Gennemsigtigt træ skabes ved at fjerne lignin fra træ og erstatte det med en polymer. Kredit:WILEY‐VCH Verlag GmbH &Co. KGaA, Weinheim, licenseret under CC BY-NC-ND 4.0 Da Timothée Boitouzet stude
Gennemsigtigt træ:fremtidens byggemateriale?Gennemsigtigt træ skabes ved at fjerne lignin fra træ og erstatte det med en polymer. Kredit:WILEY‐VCH Verlag GmbH &Co. KGaA, Weinheim, licenseret under CC BY-NC-ND 4.0 Da Timothée Boitouzet stude
- Ny forskning viser, hvordan man kan inddrage flere landmænd i udformningen af nye miljøpolitikke…
- Inside the Ink:The Science Behind Ballpoint Pens
- Nogle af verdens fattigste mennesker bærer omkostningerne ved bevarelse af tropiske skove
- Hvad er terrestriske planeter sammensætning?
- Livscyklus af en malede dame Butterfly
- Et neutralt atom, der har 8 protoner skal have?


