Propanolforbrændingsligninger:Komplet og ufuldstændig - kemi forklaret
Fuldstændig forbrænding
* Reaktanter: Propanol (C₃H₇OH) og ilt (O₂)
* Produkter: Kuldioxid (CO₂), vand (H₂O) og energi (varme)
Balanceret ligning:
2 C₃H₇OH + 9 O₂ → 6 CO₂ + 8 H₇O + Energi
Forklaring:
* Koefficienterne foran hvert molekyle sikrer, at antallet af atomer i hvert grundstof er ens på begge sider af ligningen.
* Fuldstændig forbrænding opstår, når der er nok ilt til at reagere med alt brændstoffet. Alle carbonatomer i propanol oxideres til CO₂.
Ufuldstændig forbrænding
* Reaktanter: Propanol (C₃H₇OH) og ilt (O₂)
* Produkter: Kulilte (CO), kuldioxid (CO₂), vand (H₂O) og energi (varme)
Balanceret ligning (én mulig mulighed):
2 C₃H₇OH + 7 O₂ → 4 CO₂ + 2 CO + 8 H₂O + Energi
Forklaring:
* Ufuldstændig forbrænding sker, når der ikke er nok ilt til fuldstændigt at oxidere brændstoffet.
* Dette fører til dannelsen af kulilte (CO), en giftig gas, udover kuldioxid.
* Det nøjagtige forhold mellem produceret CO₂ og CO kan variere afhængigt af ilttilgængeligheden.
Vigtig bemærkning: Ufuldstændig forbrænding er mindre effektiv med hensyn til frigivet energi og producerer skadelige biprodukter. Det er generelt uønsket, især i lukkede rum.
 Varme artikler
Varme artikler
-
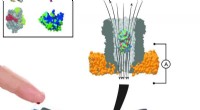 Ny metode måler enkelte molekyler fra nanoliter blod i realtidEn nanopore-enhed kan indeholde forskellige bindingsproteiner. En gang inde i poren, disse proteiner fungerer som transducere til at identificere specifikke små molekyler i en prøve af kropsvæske. Kre
Ny metode måler enkelte molekyler fra nanoliter blod i realtidEn nanopore-enhed kan indeholde forskellige bindingsproteiner. En gang inde i poren, disse proteiner fungerer som transducere til at identificere specifikke små molekyler i en prøve af kropsvæske. Kre -
 Hvordan positive og negative ioner dannes:En klar guideAf Evelyn Trimborn, opdateret 24. marts 2022 Atomer består af protoner, neutroner og elektroner. Protoner bærer en positiv ladning, neutroner er neutrale, og elektroner bærer en negativ ladning. Elek
Hvordan positive og negative ioner dannes:En klar guideAf Evelyn Trimborn, opdateret 24. marts 2022 Atomer består af protoner, neutroner og elektroner. Protoner bærer en positiv ladning, neutroner er neutrale, og elektroner bærer en negativ ladning. Elek -
 Sporing af proteinpatruljereEn nanoprobe udviklet af biofysikere ved NC State kunne give forskere mulighed for at spore bevægelserne af forskellige proteiner langs DNA - uden ulemperne ved de nuværende metoder. Et væld af prote
Sporing af proteinpatruljereEn nanoprobe udviklet af biofysikere ved NC State kunne give forskere mulighed for at spore bevægelserne af forskellige proteiner langs DNA - uden ulemperne ved de nuværende metoder. Et væld af prote -
 Emballage lavet af bananplanter et alternativ til a-peelingKredit:CC0 Public Domain Biologisk nedbrydelige plastik poser lavet af bananplanter lyder lidt...bananer, men et par UNSW-forskere har fundet en måde at gøre det på, og det kunne løse to industria
Emballage lavet af bananplanter et alternativ til a-peelingKredit:CC0 Public Domain Biologisk nedbrydelige plastik poser lavet af bananplanter lyder lidt...bananer, men et par UNSW-forskere har fundet en måde at gøre det på, og det kunne løse to industria
- Hvad er den kantede adskillelse mellem midten af sol og måne, set fra Jorden?
- Undersøgelsen sporer hukommelsen af jordfugtighed
- Hvad er de yderligere afstand, som forskere har været i stand til at se ind i universet?
- Hvilke tre former for stråling er fra solen?
- Hvilket udtryk beskriver forholdet mellem bier og blomstrende planter?
- Er natrium jernholdigt eller ikke jernholdigt?


