Hvordan positive og negative ioner dannes:En klar guide
Af Evelyn Trimborn, opdateret 24. marts 2022
Atomer består af protoner, neutroner og elektroner. Protoner bærer en positiv ladning, neutroner er neutrale, og elektroner bærer en negativ ladning. Elektroner kredser om kernen i skaller, og arrangementet af elektroner bestemmer, om et atom kan danne positive eller negative ioner.
Ioniseringsenergi
Ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra et atom eller molekyle. Grundstoffer, der allerede har en fuld ydre skal på otte elektroner (ædelgasserne) er typisk stabile, mens dem med færre eller mere end otte elektroner har svagere eller stærkere bindinger, som kan påvirkes af ioniseringsenergi.
Positiv ionisering
En positiv ion (kation) dannes, når et atom mister en eller flere elektroner. For eksempel har natrium (Na) 11 protoner og 11 elektroner, med en enkelt valenselektron i sin ydre skal. Denne valenselektron er svagt bundet og kan fjernes ved ioniseringsenergi, hvilket efterlader atomet med en netto positiv ladning:Na⁺.
Negativ ionisering
En negativ ion (anion) dannes, når et atom får en elektron. Fluor (F), med syv valenselektroner, er meget elektronegativt. Når den accepterer en ekstra elektron, fuldender den sin oktet og bærer en netto negativ ladning:F⁻.
I begge tilfælde ændrer ioniseringsprocessen elektrontallet, hvilket ændrer atomets ladning, samtidig med at dets overordnede identitet bevares.
 Varme artikler
Varme artikler
-
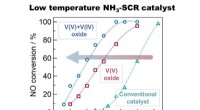 Nye katalysatorer fjerner nitrogenoxidforurenende stoffer ved lavere temperaturerOmdannelseshastighed for nitrogenoxider ved forskellige temperaturer for konventionelle, V (V) oxid og V (IV)+V (V) oxid defekte katalysatorer. Blandingen af V (V) og V (IV) oxider viste en 10 gange
Nye katalysatorer fjerner nitrogenoxidforurenende stoffer ved lavere temperaturerOmdannelseshastighed for nitrogenoxider ved forskellige temperaturer for konventionelle, V (V) oxid og V (IV)+V (V) oxid defekte katalysatorer. Blandingen af V (V) og V (IV) oxider viste en 10 gange -
 Forbedring af fremtidens oprensning ved at bruge molekylær silhuet til at adskille forbindelser i v…Holdet, ledet af professor Mohamed Eddaoudi, designede deres porøse membran til at adskille nitrogen fra metan ved at udnytte forskellen mellem gassernes molekylære form. Kredit:KAUST. Urene kemisk
Forbedring af fremtidens oprensning ved at bruge molekylær silhuet til at adskille forbindelser i v…Holdet, ledet af professor Mohamed Eddaoudi, designede deres porøse membran til at adskille nitrogen fra metan ved at udnytte forskellen mellem gassernes molekylære form. Kredit:KAUST. Urene kemisk -
 Sundere mejeriprodukter med bakteriefilm og nanofibermembranerKredit:American Chemical Society Bakterielle biofilm er typisk målet for kraftige rengøringsregimer, men disse film er ikke altid dårlige nyheder. Faktisk, at dyrke dem på tynde plader af nanofibr
Sundere mejeriprodukter med bakteriefilm og nanofibermembranerKredit:American Chemical Society Bakterielle biofilm er typisk målet for kraftige rengøringsregimer, men disse film er ikke altid dårlige nyheder. Faktisk, at dyrke dem på tynde plader af nanofibr -
 Elbiler:Særlige farvestoffer kan forhindre unødvendige motorudskiftningerFarvestoffet tilsat harpikssystemet ændrer farve, når en alkohol, der frigives af harpiksen, binder sig til det. Kredit:Uni Halle/Alexander Funtan En dag i den nærmeste fremtid kan farvestoffer i
Elbiler:Særlige farvestoffer kan forhindre unødvendige motorudskiftningerFarvestoffet tilsat harpikssystemet ændrer farve, når en alkohol, der frigives af harpiksen, binder sig til det. Kredit:Uni Halle/Alexander Funtan En dag i den nærmeste fremtid kan farvestoffer i
- Virus, orkansæson forsinkelse fjernelse af ødelagt lastskib
- Hvad udgør jordskorpe?
- Hvordan genbrug faktisk sorteres, og hvorfor Australien er ret dårlig til det
- Varmere temperaturer forårsager fald i de vigtigste afstrømningsforanstaltninger
- Hvad er Gamma Ray, der udsender genstande på Jorden?
- Afsløring af Triceratops-holdningen:En lidt kendt debat afsløret


