Molaritetsberegning:Bestemmelse af koncentrationen af H2SO4-opløsning
1. Find den molære masse af H2SO4:
* H:1,01 g/mol (x 2 =2,02 g/mol)
* S:32,07 g/mol
* O:16,00 g/mol (x 4 =64,00 g/mol)
* Total molær masse =2,02 + 32,07 + 64,00 =98,09 g/mol
2. Konverter gram H2SO4 til mol:
* Mol =(gram opløst stof) / (molær masse af opløst stof)
* Mol =18,0 g / 98,09 g/mol =0,1836 mol
3. Beregn molariteten:
* Molaritet (M) =(mol opløst stof) / (liter opløsning)
* Molaritet =0,1836 mol / 2,00 L =0,0918 M
Derfor er opløsningens molaritet 0,0918 M.
Sidste artikelBeregning af mol af H2SO4:En trin-for-trin guide
Næste artikelBeregning af normaliteten af H₂SO4:En trin-for-trin guide
 Varme artikler
Varme artikler
-
 Ny opdagelse af en så stærk fotobase, det fortjener moniker af superEn ny opdagelse af en lysinduceret superfotobase ved Michigan State University afslører nogle af fotosyntesens ønskelige træk. Det tværfaglige team af forskere var i stand til at dokumentere den super
Ny opdagelse af en så stærk fotobase, det fortjener moniker af superEn ny opdagelse af en lysinduceret superfotobase ved Michigan State University afslører nogle af fotosyntesens ønskelige træk. Det tværfaglige team af forskere var i stand til at dokumentere den super -
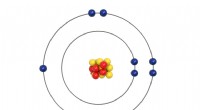 Hvordan valenselektroner bestemmer grundstofgrupper i det periodiske systemI 1869 udgav DmitriMendeleev Om forholdet mellem grundstoffernes egenskaber og deres atomvægt, der lagde grundlaget for det periodiske system. Elementer og atomvægt Under Mendeleevs æra blev atomer b
Hvordan valenselektroner bestemmer grundstofgrupper i det periodiske systemI 1869 udgav DmitriMendeleev Om forholdet mellem grundstoffernes egenskaber og deres atomvægt, der lagde grundlaget for det periodiske system. Elementer og atomvægt Under Mendeleevs æra blev atomer b -
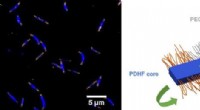 Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en
Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en -
 Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo
Farveændringstest for at hjælpe kræftforskningen videreKredit:shapecharge iStock En simpel farveændringstest til at hjælpe videnskabsmænd med at undersøge potentielle kræftlægemidler er blevet udviklet af University of Bath-forskere, gør det muligt fo
- Består gener af DNA?
- Mickey og matematik? Disney lancerer uddannelsesapps
- Team udvikler nyt materiale til bærbare enheder, der er i stand til at gendanne ledningsevne
- Forskere foreslår en ny metode til at verificere eksistensen af Majorana fermioner
- Ekstreme nedbørshændelser er forbundet over hele verden
- Hvilke faktorer påvirker biodiversiteten af et økosystem?


