Hvordan valenselektroner bestemmer grundstofgrupper i det periodiske system
I 1869 udgav DmitriMendeleev "Om forholdet mellem grundstoffernes egenskaber og deres atomvægt", der lagde grundlaget for det periodiske system.
Elementer og atomvægt
Under Mendeleevs æra blev atomer betragtet som udelelige enheder, hvis vægt varierede. At bestille elementer ved at øge vægten virkede logisk, men alligevel dukkede to nøglespørgsmål op:at måle nøjagtige atomvægte var udfordrende, og atomvægt afspejler ikke det sande organiserende princip for elementer.
Elementer og kemiske egenskaber
Mendeleev bemærkede, at "arrangement efter atomvægt svarer til grundstoffets valens og til en vis grad forskellen i kemisk adfærd." Han parrede atomvægtrækkefølge med fælles valenser og grupperede elementer med lignende egenskaber i lodrette søjler - nutidens "grupper". Dette periodiske mønster gjorde tabellen prædiktiv, hvilket gjorde det muligt for Mendeleev at forudse uopdagede elementer.
Atomstruktur
Næsten fem årtier senere udviklede atommodellen sig. Forskere opdagede en central kerne indeholdende protoner og neutroner, omgivet af en sky af elektroner. Antallet af protoner – kaldet atomnummeret – bestemmer grundstoffets identitet, og det næsten lige store antal elektroner styrer dets kemi.
Valenselektroner
Elektroner optager koncentriske skaller. Den yderste skals elektroner, kendt som valenselektroner, dikterer, hvordan et grundstof reagerer. Gruppe 1A-elementer har en enkelt valenselektron; hver efterfølgende kolonne til højre tilføjer en mere. Mens GroupB-elementer udviser mere komplekse elektronkonfigurationer, følger de også et valens-elektronmønster, som understøtter det moderne periodiske systems struktur.
Som autoritativ reference definerer International Union of Pure and Applied Chemistry (IUPAC) det periodiske system efter atomnummer, hvilket afspejler det elektronarrangement, der styrer kemisk adfærd.
Emilija Randjelovic/iStock/GettyImages
 Varme artikler
Varme artikler
-
 Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n
Lyser vejen til forbedrede biomaterialerKredit:Sleiman Lab Forskere fra McGill University mener, at de har fundet en måde at forbedre udviklingen af biomaterialer, der kunne være medvirkende til lægemiddellevering, vævsregenerering, n -
 Forstå hvorfor regn er naturligt surtAf Robert Balun Opdateret 24. marts 2022 Willowpix/iStock/GettyImages Ikke al regn kan betragtes som rent vand. Rent vand er hverken basisk eller surt. Når der falder regn fra atmosfæren, ændrer d
Forstå hvorfor regn er naturligt surtAf Robert Balun Opdateret 24. marts 2022 Willowpix/iStock/GettyImages Ikke al regn kan betragtes som rent vand. Rent vand er hverken basisk eller surt. Når der falder regn fra atmosfæren, ændrer d -
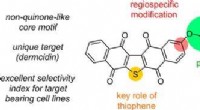 Havvandsbakterier giver fører til bekæmpelse af melanomKredit:American Chemical Society Malignt melanom kan være en særlig farlig form for kræft, og flere terapeutiske muligheder er nødvendige. Nu, forskere rapporterer i ACS Medicinal Chemistry Lette
Havvandsbakterier giver fører til bekæmpelse af melanomKredit:American Chemical Society Malignt melanom kan være en særlig farlig form for kræft, og flere terapeutiske muligheder er nødvendige. Nu, forskere rapporterer i ACS Medicinal Chemistry Lette -
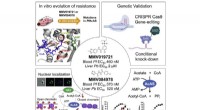 Biologiske ingeniører finder et nyt mål for malariamedicinGrafisk abstrakt. Kredit:DOI:10.1016/j.chembiol.2021.07.010 Hvert år, mere end 200 millioner mennesker er smittet med malaria, og næsten 500, 000 dør af sygdommen. Eksisterende lægemidler kan beha
Biologiske ingeniører finder et nyt mål for malariamedicinGrafisk abstrakt. Kredit:DOI:10.1016/j.chembiol.2021.07.010 Hvert år, mere end 200 millioner mennesker er smittet med malaria, og næsten 500, 000 dør af sygdommen. Eksisterende lægemidler kan beha
- Sådan får du gratis CDL træning
- Hvad er de to kræfter involveret, når en stor tung kasse hviler på fladt gulv?
- Forskere indser lydløs foton-ekko-protokol
- Hvilken type molekyle er der behov for for at danne proteinmolekyler?
- Er dehydrerede løg forbindelser eller blandinger?
- Hvorfor opvarmning af land forskellige hav?


