Hvordan salt sænker vandets frysepunkt - Videnskaben bag issmeltning
Af Juliet Myfanwy Johnson | Opdateret 24. marts 2022
Fryser
Frysepunktet for rent vand er 0°C (32°F). Ved denne temperatur er den kinetiske energi af vandmolekyler lav nok til, at de kan arrangeres i et fast gitter, der danner is. Processen er afbalanceret:Vand smelter og fryser på samme tid.
Hvordan salt sænker frysepunktet
Når salt (NaCl) indføres i systemet, dissocieres det til natrium- og chloridioner. Disse ioner forstyrrer vandmolekylernes evne til at tilpasse sig den krystallinske struktur af is, hvilket effektivt sænker temperaturen, hvorved den faste fase kan dannes. Dette fænomen, kendt som frysepunktsdepression, betyder, at isen fortsætter med at smelte, mens hastigheden af ny isdannelse aftager.
Hvorfor is smelter, før den dannes
Fordi frysepunktet er sænket, forbliver vandet i flydende tilstand selv ved temperaturer, der normalt ville fryse det. Som følge heraf dominerer smeltningsprocessen, og den is, der findes, er mindre stabil, hvilket fører til en nettoreduktion i istykkelsen.
Andre opløsninger virker på samme måde
Ethvert opløst stof - såsom alkohol, sukker eller andre kemikalier - kan forstyrre ligevægten af vandmolekyler på samme måde. Salt er det mest almindelige valg til afisning af veje på grund af dets lave omkostninger, høje tilgængelighed og effektivitet til at reducere vandets frysepunkt med flere grader.
Praktiske applikationer
Vejpersonale spreder salt på isglatte overflader for at skabe et saltlage, der forbliver flydende ved temperaturer under frysepunktet. Dette smelter ikke kun eksisterende is, men forhindrer også ny is i at dannes, indtil temperaturen stiger over det lave frysepunkt.
For mere detaljerede videnskabelige forklaringer, konsulter peer-reviewede undersøgelser af kolligative egenskaber og faseovergange i vandige opløsninger.
 Varme artikler
Varme artikler
-
 Kamæleonlignende materiale tilsat bor kommer tættere på at efterligne hjernecellerHvert vågent øjeblik, vores hjerne behandler en enorm mængde data for at give mening om omverdenen. Dermed, ved at efterligne den måde, den menneskelige hjerne løser hverdagens problemer, neuromorfe s
Kamæleonlignende materiale tilsat bor kommer tættere på at efterligne hjernecellerHvert vågent øjeblik, vores hjerne behandler en enorm mængde data for at give mening om omverdenen. Dermed, ved at efterligne den måde, den menneskelige hjerne løser hverdagens problemer, neuromorfe s -
 Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer
Bakterier fodret på en tilpasset diæt producerer biologisk nedbrydelige polymerer til alternativ e…Frysetørrede bakterier (Cupriavidus necator) før celleafbrydelse. Kredit:Fraunhofer-Gesellschaft Tyskland genererer omkring 38 kg plastaffald pr. indbygger hvert år. I et fælles projekt med Univer -
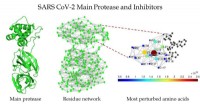 Målretning af SARS-CoV-2-enzym med inhibitorerSkematisk af hovedproteasen af SARS CoV-2 (venstre), proteinrestnetværket af hovedproteasen i SARS CoV-2 (i midten), og en zoomet visning af området omkring bindingsstedet som detekteret af Estrada
Målretning af SARS-CoV-2-enzym med inhibitorerSkematisk af hovedproteasen af SARS CoV-2 (venstre), proteinrestnetværket af hovedproteasen i SARS CoV-2 (i midten), og en zoomet visning af området omkring bindingsstedet som detekteret af Estrada -
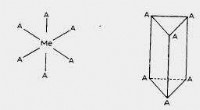 Molekylær struktur forudsagt af den tidlige nobelpristager fundet efter et århundredeKredit:Kilde:Nobelforelæsning af Alfred Werner 11. december, 1913 fra det originale papir nobelprize.org I journalen Natur udgivet natten over, forskere fra Imperial College, London har rapporte
Molekylær struktur forudsagt af den tidlige nobelpristager fundet efter et århundredeKredit:Kilde:Nobelforelæsning af Alfred Werner 11. december, 1913 fra det originale papir nobelprize.org I journalen Natur udgivet natten over, forskere fra Imperial College, London har rapporte
- Partikels bølgeegenskaber kan manifestere sig ved kollisioner
- Sådan fungerer biodynamisk landbrug
- Ændrer ikke en stoffer identitet fysisk eller kemisk ændring?
- Undersøgelser sætter gang i debatten om, hvorfor hunfugle søger ekstra makker
- 4S Orbital er fyldt før 3D Orbital?
- Hvad er det modsatte abstrakte substantiv for opdagelse?


