Kovalente bindinger:Forståelse af elektrondeling i atomer
Her er en oversigt:
* Ydre skal (Valence Shell): Den yderste elektronskal af et atom.
* Elektroner: Negativt ladede partikler, der kredser om kernen i et atom.
* Deling: Når to atomer deler elektroner, skaber de et stabilt arrangement, hvor begge atomer har en fuld ydre skal, der efterligner ædelgaskonfigurationen.
Eksempler på kovalente bindinger:
* Vand (H2O): Iltatomet deler to elektroner med to hydrogenatomer.
* Kuldioxid (CO2): Kulstofatomet deler fire elektroner med to oxygenatomer.
* Metan (CH4): Kulstofatomet deler fire elektroner med fire brintatomer.
Nøglepunkter:
* Kovalente bindinger er typisk stærkere end ionbindinger (hvor elektroner overføres).
* De kan være enkelt-, dobbelt- eller tredobbeltbindinger, afhængigt af antallet af delte elektroner.
* Kovalente bindinger er ansvarlige for dannelsen af langt de fleste organiske molekyler, inklusive dem, der findes i levende organismer.
Lad mig vide, hvis du vil have flere eksempler eller detaljer om kovalent binding!
 Varme artikler
Varme artikler
-
 Ingeniører 3D-print med formskiftende smart gelEn lille skak konge, 3D-printet med en temperaturfølsom hydrogel, i koldt vand. Den indeholder 73 procent vand, men forbliver fast. Kredit:Daehoon Han/Rutgers University-New Brunswick Rutgers inge
Ingeniører 3D-print med formskiftende smart gelEn lille skak konge, 3D-printet med en temperaturfølsom hydrogel, i koldt vand. Den indeholder 73 procent vand, men forbliver fast. Kredit:Daehoon Han/Rutgers University-New Brunswick Rutgers inge -
 Forskning i retning af levedygtige, sikre batterier overvinder høj modstand, solid-state barrierer …Kredit:A. James Clark School of Engineering, University of Maryland Ingeniører ved University of Maryland har udviklet et middel til at overvinde forhindringer i udviklingen af solid-state batte
Forskning i retning af levedygtige, sikre batterier overvinder høj modstand, solid-state barrierer …Kredit:A. James Clark School of Engineering, University of Maryland Ingeniører ved University of Maryland har udviklet et middel til at overvinde forhindringer i udviklingen af solid-state batte -
 Elektriske vs. traditionelle bilbatterier:Vigtigste forskelle forklaretBLKstudio/Shutterstock På nutidens veje dominerer to adskilte køretøjskategorier:elektriske køretøjer (EVer) og konventionelle forbrændingsmotorer (ICE) biler. Selvom de deler et fælles mål – at tran
Elektriske vs. traditionelle bilbatterier:Vigtigste forskelle forklaretBLKstudio/Shutterstock På nutidens veje dominerer to adskilte køretøjskategorier:elektriske køretøjer (EVer) og konventionelle forbrændingsmotorer (ICE) biler. Selvom de deler et fælles mål – at tran -
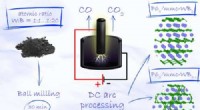 Superhård materialesyntese gjort billigereGrafisk abstrakt. Kredit:Uorganisk kemi (2022). DOI:10.1021/acs.inorgchem.1c03880 Skoltech-forskere og deres kolleger fra Tomsk Polytechnic University har foreslået en effektiv og billig måde at sy
Superhård materialesyntese gjort billigereGrafisk abstrakt. Kredit:Uorganisk kemi (2022). DOI:10.1021/acs.inorgchem.1c03880 Skoltech-forskere og deres kolleger fra Tomsk Polytechnic University har foreslået en effektiv og billig måde at sy
- Konstruktion af hule nanoreaktorer til forbedrede fotooxidationer
- Der kunne være fremmede liv på Mars, men vil vores rovere være i stand til at finde det?
- Jordens vand kan oprindeligt være blevet dannet dybt inde i dens kappe, viser undersøgelse
- Giv de vigtigste videnskabsgrene?
- Hvem brugte et teleskop til at opdage kratere på månen?
- Hvad er grundfjeldjord?


