Forståelse af vands flydende tilstand:rollen af brintbindinger
* Polaritet: Vandmolekyler er polære, hvilket betyder, at de har en let positiv ende (brintatomer) og en lidt negativ ende (iltatom). Denne polaritet opstår fra forskellen i elektronegativitet mellem oxygen og brint.
* Brintbinding: Den positive ende af et vandmolekyle tiltrækkes af den negative ende af et andet vandmolekyle. Denne stærke elektrostatiske interaktion, kaldet hydrogenbinding, er meget stærkere end de dipol-dipolkræfter, der findes i andre polære molekyler.
* Netværk af obligationer: Hydrogenbindinger skaber et netværk af indbyrdes forbundne vandmolekyler, der holder dem tættere sammen end de svagere kræfter, der er til stede i andre væsker. Dette stærke netværk kræver en betydelig mængde energi for at bryde, hvorfor vand har et relativt højt kogepunkt og er flydende ved stuetemperatur.
Andre faktorer:
Mens hydrogenbinding er den primære årsag, spiller andre intermolekylære kræfter også en rolle:
* Dipol-dipolkræfter: Disse svagere kræfter eksisterer også mellem polære vandmolekyler.
* Spredningskræfter i London: Disse meget svage kræfter eksisterer mellem alle molekyler, inklusive vand.
Opsummering: Den stærke hydrogenbinding mellem vandmolekyler, kombineret med de andre intermolekylære kræfter, er ansvarlig for vands flydende tilstand ved stuetemperatur.
Sidste artikelArgon Gas:Atomer vs. Molecules - Forståelse af atomstruktur
Næste artikelVand og temperatur:Hydrogenbindingernes rolle
 Varme artikler
Varme artikler
-
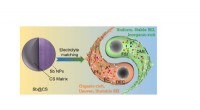 Opnåelse af stabil K-lagringsydelse af carbonkugle-begrænset antimon via elektrolytreguleringDen interne mikrostruktur af Sb@CS med ensartet fordeling af C og Sb udviser helt forskellige egenskaber i to typiske elektrolytter, men den elektrokemiske ydeevne kan opretholde stabilitet efter elek
Opnåelse af stabil K-lagringsydelse af carbonkugle-begrænset antimon via elektrolytreguleringDen interne mikrostruktur af Sb@CS med ensartet fordeling af C og Sb udviser helt forskellige egenskaber i to typiske elektrolytter, men den elektrokemiske ydeevne kan opretholde stabilitet efter elek -
 Denatureret alkohol vs. isopropylalkohol:Produktion, sikkerhed og anvendelserAf Doug Johnson Opdateret 30. august 2022 PRImageFactory/iStock/GettyImages I kemi refererer alkohol til en bred klasse af organiske forbindelser, der indeholder mindst én hydroxylgruppe (-OH). Men
Denatureret alkohol vs. isopropylalkohol:Produktion, sikkerhed og anvendelserAf Doug Johnson Opdateret 30. august 2022 PRImageFactory/iStock/GettyImages I kemi refererer alkohol til en bred klasse af organiske forbindelser, der indeholder mindst én hydroxylgruppe (-OH). Men -
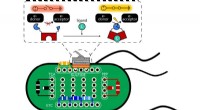 Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen
Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen -
 Nyt materiale kan spare tid og penge inden for medicinsk billeddannelse og miljøsaneringHumphrey og hans team er ved at udvikle oliepinde til papir, der hurtigt og billigt kan identificere en lang række kemikalier i en ukarakteriseret prøve. Hvert kemikalie producerer en unik otte-faktor
Nyt materiale kan spare tid og penge inden for medicinsk billeddannelse og miljøsaneringHumphrey og hans team er ved at udvikle oliepinde til papir, der hurtigt og billigt kan identificere en lang række kemikalier i en ukarakteriseret prøve. Hvert kemikalie producerer en unik otte-faktor
- Mystiske udbrud af energi kommer fra det ydre rum
- Hvilke oplysninger transmitterer Voyager Space -sonderne?
- Hvilken af følgende luftforurenende stoffer er ikke en primær forurening?
- Deodoranttilstand:Fast vs. Gas - Forstå hvad der er indeni
- Ny indsigt om de lyseste eksplosioner i universet
- Kan du ikke konkurrere på møg? Prøv at parre æblepresser


