Forståelse af oxidationstal:Et praktisk eksempel (NaCl)
Eksempel på oxidationsnummer:
Lad os tage forbindelsen Natriumchlorid (NaCl)
1. Identificer elementerne: Vi har natrium (Na) og klor (Cl).
2. Anvend regler:
* Regel 1: Oxidationstallet for et grundstof i dets grundstofform er altid nul.
* Regel 2: Alkalimetaller (som natrium) har altid et oxidationstal på +1 i forbindelser.
* Regel 3: Halogener (som klor) har normalt et oxidationstal på -1 i forbindelser.
3. Tildel oxidationsnumre:
* Natrium (Na) har et oxidationstal på +1 .
* Klor (Cl) har et oxidationstal på -1 .
Derfor er oxidationstallene i NaCl +1 for natrium og -1 for klor.
Forklaring:
Natrium er i gruppe 1, hvilket betyder, at det har en valenselektron, som det let giver op for at opnå en stabil oktet. Klor er i gruppe 17 og har brug for en elektron for at fuldføre sin oktet. Når de binder, mister natrium en elektron (bliver +1), og klor vinder den elektron (bliver -1).
Nøglepunkter:
* Oxidationstal er et bogføringsværktøj til at spore elektronbevægelser i kemiske reaktioner.
* De er ikke faktiske ladninger, men snarere en måde at repræsentere den hypotetiske ladning et atom ville have, hvis alle bindinger var ioniske.
* Summen af oxidationstal i en neutral forbindelse skal være lig med nul.
* Et grundstofs oxidationsnummer kan variere afhængigt af den forbindelse, det er i.
Sidste artikelBlandinger:Forståelse af fysiske kombinationer af stoffer
Næste artikelForståelse af argonkemi:egenskaber og reaktioner
 Varme artikler
Varme artikler
-
 En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere
En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere -
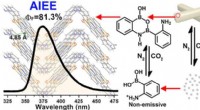 Nyt aggregationsinduceret aromatisk molekyle med forbedret emission opdaget2-APBA-dimeren, der har tendens til at aggregere til en meget ordnet struktur, er AIEE-aktiv. Kredit:LI Xiaopei Aggregations-inducerede molekyler med øget emission (AIEE), nye selvlysende material
Nyt aggregationsinduceret aromatisk molekyle med forbedret emission opdaget2-APBA-dimeren, der har tendens til at aggregere til en meget ordnet struktur, er AIEE-aktiv. Kredit:LI Xiaopei Aggregations-inducerede molekyler med øget emission (AIEE), nye selvlysende material -
 Comet inspirerer til kemi til fremstilling af åndbar ilt på MarsKonstantinos P. Giapis med sin reaktor, der omdanner kuldioxid til molekylær oxygen. Kredit:California Institute of Technology Science fiction-historier er fyldt med terraforming-skemaer og iltgen
Comet inspirerer til kemi til fremstilling af åndbar ilt på MarsKonstantinos P. Giapis med sin reaktor, der omdanner kuldioxid til molekylær oxygen. Kredit:California Institute of Technology Science fiction-historier er fyldt med terraforming-skemaer og iltgen -
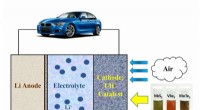 2-D-materialer kan gøre det muligt for elektriske køretøjer at komme 500 miles på en enkelt opla…2D-katalysatorer driver et elektrisk køretøj. Kredit:Amin Salehi-Khojin Lithium-luft-batterier er klar til at blive den næste revolutionerende erstatning for aktuelt brugte lithium-ion-batterier,
2-D-materialer kan gøre det muligt for elektriske køretøjer at komme 500 miles på en enkelt opla…2D-katalysatorer driver et elektrisk køretøj. Kredit:Amin Salehi-Khojin Lithium-luft-batterier er klar til at blive den næste revolutionerende erstatning for aktuelt brugte lithium-ion-batterier,
- Hvorfor udforsker mennesker i rummet?
- Vedvarende høje pesticidniveauer fundet i små vandløb
- Peer indflydelse, sociale netværk kan blive udnyttet til at støtte bestræbelserne på at reducere…
- Cellegenskaber
- I begyndelsen af eukaryotisk cellecyklus vokser og duplikerer dens.?
- Hvilken slags celler gengiver gennem processen meiose?


