Forstå bindingen mellem ilt og brint
* Elektronegativitet: Ilt har en højere elektronegativitet end brint. Det betyder, at ilt har en stærkere tiltrækning af elektroner end brint.
* Kovalent binding: I en kovalent binding deler atomer elektroner for at opnå en stabil elektronkonfiguration. Ilt har brug for to elektroner mere for at fylde sin ydre skal, mens brint har brug for en. Ved at dele elektroner opnår de begge en stabil konfiguration.
Sådan virker det:
1. Deling af elektroner: Når et oxygenatom og to brintatomer kommer sammen, deler de elektroner. Hvert brintatom deler sin enkelte elektron med oxygenatomet, og oxygenatomet deler en af sine elektroner med hvert brintatom.
2. Stabil konfiguration: Denne deling af elektroner resulterer i en stabil konfiguration for både oxygen og brint. Ilt har en fuld ydre skal på otte elektroner, mens hvert brintatom har en fuld ydre skal på to elektroner.
3. Polær kovalent binding: Bindingen mellem oxygen og hydrogen er en polær kovalent binding . Det betyder, at de delte elektroner ikke deles ligeligt mellem atomerne. Iltatomet trækker elektronerne tættere på sig selv på grund af dets højere elektronegativitet. Dette giver oxygenatomet en let negativ ladning og brintatomerne en let positiv ladning.
Resultatet er dannelsen af vand (H₂O), et molekyle, der er afgørende for livet.
Opsummering: Elektronegativitetsforskellen mellem oxygen og brint, sammen med dannelsen af en kovalent binding, tillader dem at binde sammen og danne vand.
 Varme artikler
Varme artikler
-
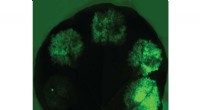 Nye syntetiske biologiværktøjer låser op for kompleks anlægsteknikEt blad med forskellige syntetiske promotorer, der udtrykker grønt fluorescerende protein, demonstrerer rækken af ekspressionsniveauer, der kan opnås med deres konstruerede promotorer. Kredit:JBEI/B
Nye syntetiske biologiværktøjer låser op for kompleks anlægsteknikEt blad med forskellige syntetiske promotorer, der udtrykker grønt fluorescerende protein, demonstrerer rækken af ekspressionsniveauer, der kan opnås med deres konstruerede promotorer. Kredit:JBEI/B -
 Kan citronsyre være et grønt alternativ til beskyttelse af stål?Citronsyre som grønt alternativ til metalbeskyttelsesmiddel. Kredit:European Space Agency Salpetersyre er i øjeblikket den mest anvendte passiveringsløsning til beskyttelse af rustfrit stål mod ko
Kan citronsyre være et grønt alternativ til beskyttelse af stål?Citronsyre som grønt alternativ til metalbeskyttelsesmiddel. Kredit:European Space Agency Salpetersyre er i øjeblikket den mest anvendte passiveringsløsning til beskyttelse af rustfrit stål mod ko -
 Nye katalysatorer efterligner menneskesynLilla LEDer aktiverer denne nye katalysator designet hos ICIQ. Kredit:Public domain Fotoreceptorer hos hvirveldyr består typisk af to separate farveløse dele:et organisk pigment og et protein. Kom
Nye katalysatorer efterligner menneskesynLilla LEDer aktiverer denne nye katalysator designet hos ICIQ. Kredit:Public domain Fotoreceptorer hos hvirveldyr består typisk af to separate farveløse dele:et organisk pigment og et protein. Kom -
 Fjernelse af fugt fra naturgas:en teknisk oversigtAf David Hoskins, Opdateret 24. marts 2022 Naturgas leverer omkring 24% af USAs energibehov. Inden den når forbrugerne, raffineres gassen til en metanstrøm med høj renhed. Et nøgletrin i denne forfin
Fjernelse af fugt fra naturgas:en teknisk oversigtAf David Hoskins, Opdateret 24. marts 2022 Naturgas leverer omkring 24% af USAs energibehov. Inden den når forbrugerne, raffineres gassen til en metanstrøm med høj renhed. Et nøgletrin i denne forfin
- Hvad opretholder Jordens magnetfelt overhovedet?
- Hvordan reagerer bakteriesamfund i sort jord på konventionel og biologisk nedbrydelig mikroplast?
- Pakistan er ligeglad, da smog dræber flere mennesker end militante
- Hvordan konverterer du celsius til farenheith?
- Karboner Atomnummer Protoner Neutroner og elektroner?
- Er det sandt eller falskt et vibrerende objekt skubber molekylerne sammen og forårsager et komprime…


