Valence Shell &Chemical Bonding:Forståelse af molekylær dannelse
* Valenselektroner: Disse er elektronerne i den yderste skal af et atom. Det er dem, der er involveret i kemisk binding.
* Oktetregel: De fleste atomer stræber efter at opnå en stabil konfiguration med otte elektroner i deres valensskal (bortset fra brint og helium, som sigter mod to).
* Binding: Atomer kan opnå denne stabile konfiguration ved enten:
* Deling af elektroner: Dette kaldes kovalent binding og danner molekyler.
* Overførsel af elektroner: Dette kaldes ionisk binding og danner ioniske forbindelser.
Her er en forenklet forklaring:
1. Atomer med færre end otte valenselektroner (eller to for hydrogen og helium) er reaktive. De ønsker at vinde eller miste elektroner for at fylde deres yderste skal.
2. Atomer med mere end fire valenselektroner er mere tilbøjelige til at få elektroner.
3. Atomer med færre end fire valenselektroner er mere tilbøjelige til at miste elektroner.
4. Atomer deler eller overfører elektroner for at opnå en stabil konfiguration. Dette resulterer i dannelsen af bindinger og molekyler.
Eksempler:
* Oxygen (O): Den har seks valenselektroner. For at opnå en stabil oktet vil den danne to kovalente bindinger ved at dele to elektroner med et andet atom (som i O2).
* Natrium (Na): Den har en valenselektron. For at opnå en stabil oktet vil den miste den elektron og blive en positivt ladet ion (Na+).
* Klor (Cl): Det har syv valenselektroner. Den vil få en elektron for at opnå en stabil oktet, der bliver en negativt ladet ion (Cl-). Den resulterende binding mellem Na+ og Cl- danner natriumchlorid (NaCl), et almindeligt salt.
Så valensskallen og antallet af valenselektroner har direkte indflydelse på, hvordan atomer vil interagere og bindes for at danne molekyler.
 Varme artikler
Varme artikler
-
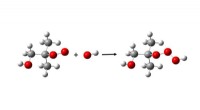 Ny type ekstremt reaktivt stof opdaget i atmosfærenReaktion:ROO + OH → ROOOH (iltatomer i rødt). Kredit:Københavns Universitet For første gang er en helt ny klasse af superreaktive kemiske forbindelser blevet opdaget under atmosfæriske forhold. For
Ny type ekstremt reaktivt stof opdaget i atmosfærenReaktion:ROO + OH → ROOOH (iltatomer i rødt). Kredit:Københavns Universitet For første gang er en helt ny klasse af superreaktive kemiske forbindelser blevet opdaget under atmosfæriske forhold. For -
 Hvorfor alkoholer koger højere end alkaner med lignende molær masseMolar masse og kogepunkt Kogepunktet stiger generelt med stigende molmasse, fordi større molekyler har stærkere London-spredningskræfter. Men når man sammenligner molekyler med næsten identisk molær
Hvorfor alkoholer koger højere end alkaner med lignende molær masseMolar masse og kogepunkt Kogepunktet stiger generelt med stigende molmasse, fordi større molekyler har stærkere London-spredningskræfter. Men når man sammenligner molekyler med næsten identisk molær -
 To bakterielle co-kulturer øger mikrobe co-nedbrydning af dicarboximid fungiciderGrafisk abstrakt. https://doi.org/10.1016/j.jhazmat.2020.123888 Dicarboximid fungicider dimethachlon, iprodion og procymidon er blevet meget brugt over hele verden til at kontrollere plantesygdomm
To bakterielle co-kulturer øger mikrobe co-nedbrydning af dicarboximid fungiciderGrafisk abstrakt. https://doi.org/10.1016/j.jhazmat.2020.123888 Dicarboximid fungicider dimethachlon, iprodion og procymidon er blevet meget brugt over hele verden til at kontrollere plantesygdomm -
 Forståelse af gasflow for forbedrede anvendelser af ren energiFig.1:Strømlininger af gasstrømning gennem et porøst medium induceret af påført trykgradient ∇p. Farven på strømlinjer repræsenterer styrken af strømningshastigheden, hvor rød repræsenterer hurtig h
Forståelse af gasflow for forbedrede anvendelser af ren energiFig.1:Strømlininger af gasstrømning gennem et porøst medium induceret af påført trykgradient ∇p. Farven på strømlinjer repræsenterer styrken af strømningshastigheden, hvor rød repræsenterer hurtig h
- Udgravning af beviser på mere sofistikeret fremstilling i bronzealderen
- Hvordan begynder stjerner og afslutter deres liv?
- Lån fra naturen for at udnytte solens kraft
- Formel for ioniske forbindelser fremstillet med følgende ioner natrium- og sulfidioner?
- Forskere går sammen for at vise, at skovens biodiversitet er grøn på mere end én måde
- Hvor fungerer en stenhugger?


