Ammoniumchloriddannelse:Forståelse af reaktionsstedet
1. Diffusionshastigheder:
* Ammoniak (NH₃) er lettere end HCl: Ammoniakgas har en lavere molekylvægt end hydrogenchlorid. Det betyder, at ammoniakmolekyler bevæger sig hurtigere og diffunderer hurtigere gennem luften.
* HCl diffunderer langsommere: HCl er tungere og diffunderer langsommere.
2. Reaktionen:
* Ammoniak og HCl reagerer i luften: Når ammoniak- og HCl-gasmolekyler kolliderer, reagerer de og danner ammoniumchlorid (NH4Cl). Denne reaktion er eksoterm (frigiver varme).
3. Resultatet:
* Flere kollisioner nær HCl-enden: Da HCl diffunderer langsommere, tager det længere tid at sprede sig. Dette betyder, at der er en højere koncentration af HCl-molekyler nær HCl-enden af røret.
* Flere kollisioner betyder mere ammoniumchlorid: Fordi der er mere HCl tættere på HCl-enden, opstår der flere kollisioner, hvilket resulterer i mere ammoniumchloriddannelse nær det sted.
I det væsentlige dannes ammoniumchloridet tættere på HCl-enden, fordi HCl-gassen diffunderer langsommere og derfor skaber en tættere sky af HCl-molekyler, som ammoniakken kan reagere med.
 Varme artikler
Varme artikler
-
 Anti-degranulering og galdesyrebindende aktivitet af frugter og agroindustrielle biprodukterKredit:Anna Langova/Public Domain De ubrugte dele af frugt og grøntsager, såsom frugtkød efter juicening, indeholder ofte flere fytokemikalier med bioregulerende funktioner end de brugte dele, men
Anti-degranulering og galdesyrebindende aktivitet af frugter og agroindustrielle biprodukterKredit:Anna Langova/Public Domain De ubrugte dele af frugt og grøntsager, såsom frugtkød efter juicening, indeholder ofte flere fytokemikalier med bioregulerende funktioner end de brugte dele, men -
 Singlet oxygen nedbryder selektivt oxytetracyclin i fentonlignende oxidationMekanismediagram over Co/C+H 2 O 2 system til selektiv nedbrydning af OTC -forurenende stoffer. Kredit:HONG Peidong For nylig, et forskergruppe ledet af Prof. 2 O 2 ) for at generere singl
Singlet oxygen nedbryder selektivt oxytetracyclin i fentonlignende oxidationMekanismediagram over Co/C+H 2 O 2 system til selektiv nedbrydning af OTC -forurenende stoffer. Kredit:HONG Peidong For nylig, et forskergruppe ledet af Prof. 2 O 2 ) for at generere singl -
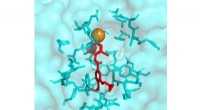 Forskere fremskynder indsatsen for at håndtere parasitiske rundormePDE -hæmmer bundet til PDE4. Kredit:UNH Rundorme, der lever af planter, forårsager årlige globale afgrødeskader på cirka 100 milliarder dollars. Nu har forskere ved University of New Hampshire gjo
Forskere fremskynder indsatsen for at håndtere parasitiske rundormePDE -hæmmer bundet til PDE4. Kredit:UNH Rundorme, der lever af planter, forårsager årlige globale afgrødeskader på cirka 100 milliarder dollars. Nu har forskere ved University of New Hampshire gjo -
 Forskere designer lovende ny katode til natriumbaserede batterierXiao-Qing Yang (til venstre) og Enyuan Hu (i midten) af Brookhavens kemiafdeling, afbildet med strålefysiker Eli Stavitski (til højre) ved ISS strålelinje ved NSLS-II. Kredit:Brookhaven National Labor
Forskere designer lovende ny katode til natriumbaserede batterierXiao-Qing Yang (til venstre) og Enyuan Hu (i midten) af Brookhavens kemiafdeling, afbildet med strålefysiker Eli Stavitski (til højre) ved ISS strålelinje ved NSLS-II. Kredit:Brookhaven National Labor
- Hvordan er medlemmer af Kingdoms Archaebacteria og Plantae, hvordan er de forskellige?
- Hvad er en urancentrifuge?
- Hvorfor er min Mercury Mystic fra 1998 langsomt at fylde op med gas?
- Er alle måner i vores solsystem tidevandslåste?
- Farve på salpetersyre i 0,1 bromthymol blå?
- Forskere skaber verdens første molekylære transistor


