Eddikesyreledningsevne:Forståelse af virkningen af koncentration
Forklaring:
* Konduktivitet er et mål for en løsnings evne til at lede elektricitet. Det er direkte proportionalt med koncentrationen af ioner i opløsningen.
* Eddikesyre (CH3COOH) er en svag syre, hvilket betyder, at den kun delvist ioniserer i opløsning. Ioniseringsligevægten er som følger:
```
CH3COOH(aq) ⇌ H+(aq) + CH3COO-(aq)
```
* Koncentreret eddikesyre indeholder en højere koncentration af eddikesyremolekyler. Dette fører til en højere koncentration af ioner (H+ og CH3COO-) i opløsning, hvilket resulterer i højere ledningsevne.
* Fortyndet eddikesyre har en lavere koncentration af eddikesyremolekyler. Koncentrationen af ioner er derfor lavere, hvilket fører til lavere ledningsevne.
Opsummering:
* Højere koncentration af eddikesyre =Højere ionisering =Flere ioner =Højere ledningsevne.
* Lavere koncentration af eddikesyre =Lavere ionisering =Færre ioner =Lavere ledningsevne.
Bemærk:
* Ledningsevnen af eddikesyreopløsninger afhænger også af faktorer som temperatur og tilstedeværelsen af andre elektrolytter.
* Ledningsevnen af koncentreret eddikesyre kan være ret høj, men den er stadig betydeligt lavere end for stærke syrer som saltsyre (HCl) på grund af dens svage sure natur.
 Varme artikler
Varme artikler
-
 Kemikere opdager en nøgle til grønnere fødevareproduktionSkinnende blåt lys på iridium gør det “ophidset, ”Giver den energi til at støde ind i antracenmolekylet og overføre et hydrogenatom, danner et svagt bånd. Iridiumkatalysatoren aktiverer derefter hydro
Kemikere opdager en nøgle til grønnere fødevareproduktionSkinnende blåt lys på iridium gør det “ophidset, ”Giver den energi til at støde ind i antracenmolekylet og overføre et hydrogenatom, danner et svagt bånd. Iridiumkatalysatoren aktiverer derefter hydro -
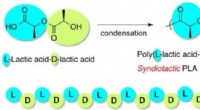 Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer
Fremgangsmåde til at syntetisere en ny polyester med alternerende arrangementFremgangsmåde til syntetisering af rene syndiotaktiske poly(mælkesyre)polyestere og billede af sfærulit deraf. Grafisk abstrakt af Polymerkemi , 2018, 9, 2446-2457. DOI:10.1039/C8PY00391B-Reproducer -
 Et klæbrigt emne:At studere skaldyr til avancerede klæbemidlerJonathan Wilker, professor i uorganisk kemi, studerer skaldyr for at udvikle klæbemidler, der er mere bæredygtige og stærkere, og arbejde i en bredere vifte af miljøer end nuværende klæbemidler. Kredi
Et klæbrigt emne:At studere skaldyr til avancerede klæbemidlerJonathan Wilker, professor i uorganisk kemi, studerer skaldyr for at udvikle klæbemidler, der er mere bæredygtige og stærkere, og arbejde i en bredere vifte af miljøer end nuværende klæbemidler. Kredi -
 Nyt materiale kan spare tid og penge inden for medicinsk billeddannelse og miljøsaneringHumphrey og hans team er ved at udvikle oliepinde til papir, der hurtigt og billigt kan identificere en lang række kemikalier i en ukarakteriseret prøve. Hvert kemikalie producerer en unik otte-faktor
Nyt materiale kan spare tid og penge inden for medicinsk billeddannelse og miljøsaneringHumphrey og hans team er ved at udvikle oliepinde til papir, der hurtigt og billigt kan identificere en lang række kemikalier i en ukarakteriseret prøve. Hvert kemikalie producerer en unik otte-faktor
- Hvad er to måder at beskrive en stjerners lysstyrke på?
- Hvordan jordskælv virker
- Forskere opdager en valleytronics-rute mod reversibel computer
- Forskning fremhæver de økonomiske omkostninger ved mobning på arbejdspladsen
- Hvordan er orions rumfartøjer og rumfærge ens?
- Hvorfor måles ikke hastigheden af elektromagnetiske bølger?


