Jernklorid:støkiometrisk vs. katalytisk brug og hvorfor
Her er hvorfor:
* Reaktioner, hvor det virker som en oxidant: Ferrichlorid bruges ofte som et oxidationsmiddel i forskellige reaktioner, såsom chlorering af aromatiske forbindelser eller oxidation af alkoholer. I disse tilfælde forbruges det under reaktionen og regenereres ikke.
* Reaktioner, hvor den virker som en Lewis-syre: Jernchlorid kan fungere som en Lewis-syre i nogle reaktioner, hvilket fremmer dannelsen af karbokationer eller aktiverer substrater. Det bruges dog typisk ikke i katalytiske mængder i disse reaktioner.
Eksempler på brug af ferrichlorid i støkiometriske mængder:
* Klorering af aromatiske forbindelser: Ferrichlorid bruges som katalysator ved chlorering af aromatiske forbindelser. Det forbruges dog i reaktionen og regenereres ikke.
* Oxidation af alkoholer: Jernchlorid kan bruges til at oxidere alkoholer til aldehyder eller ketoner. Det er et godt oxidationsmiddel, fordi det er relativt billigt og nemt at håndtere.
* Ringåbning af epoxider: Jernchlorid kan katalysere ringåbningen af epoxider. Det bruges dog ikke i katalytiske mængder, fordi det forbruges i reaktionen.
Hvor katalytiske mængder bruges:
I nogle specifikke tilfælde kan ferrichlorid bruges i katalytiske mængder, når det fungerer som en katalysator i en reaktion, hvor det regenereres, men disse er ikke almindelige anvendelser.
Vigtig bemærkning: Det er afgørende at forstå den specifikke reaktionskontekst for at bestemme, om ferrichlorid anvendes i katalytiske eller støkiometriske mængder.
 Varme artikler
Varme artikler
-
 Ny undersøgelse foreslår en lav pris, højeffektiv maskedesignKredit:CC0 Public Domain Et nyt papir ind Oxford Open Materials Science præsenterer billige modifikationer til eksisterende N95-masker, der forlænger deres effektivitet og forbedrer deres genanv
Ny undersøgelse foreslår en lav pris, højeffektiv maskedesignKredit:CC0 Public Domain Et nyt papir ind Oxford Open Materials Science præsenterer billige modifikationer til eksisterende N95-masker, der forlænger deres effektivitet og forbedrer deres genanv -
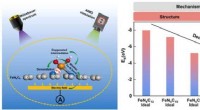 Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne
Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne -
 Neutroner kaster lys over industriel katalysator til brintproduktionSamarbejdspartnere ved Department of Energys Oak Ridge National Laboratory og amerikanske universiteter brugte neutronspredning og andre avancerede karakteriseringsteknikker til at studere, hvordan en
Neutroner kaster lys over industriel katalysator til brintproduktionSamarbejdspartnere ved Department of Energys Oak Ridge National Laboratory og amerikanske universiteter brugte neutronspredning og andre avancerede karakteriseringsteknikker til at studere, hvordan en -
 Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo
Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo
- Snacks på hjul:PepsiCo tester selvkørende robotlevering
- Radikalisering til ekstremistiske ideologier udløses ofte af negative livsbegivenheder
- Magisk vinkelgrafen og skabelsen af uventede topologiske kvantetilstande
- Når månen vokser sollysdelen?
- Hvad er navnene på celler i din hjerne?
- Hvordan bevæger phylum sporozoer sig?


