Forstå renheden af calciumoxid (CaO)
Kemisk renhed:
* Definition: Et stof er kemisk rent, når det kun indeholder de specificerede grundstoffer eller forbindelser i et defineret forhold uden urenheder eller forurenende stoffer.
* Calciumoxid: I sin ideelle form består calciumoxid udelukkende af calcium- og oxygenatomer, der overholder den kemiske formel CaO.
Praktisk renhed:
* Definition: Dette refererer til den faktiske renhed af et stof, som findes i den virkelige verden. Det tager højde for tilstedeværelsen af urenheder, selvom de er i små mængder.
* Calciumoxid: Selvom calciumoxid teoretisk er rent i sin kemiske struktur, indeholder kommercielt tilgængeligt calciumoxid ofte nogle urenheder som:
* Fugt: Calciumoxid er hygroskopisk, hvilket betyder, at det let absorberer fugt fra luften og danner calciumhydroxid (Ca(OH)2).
* Kuldioxid: Calciumoxid reagerer med kuldioxid i luften og danner calciumcarbonat (CaCO3).
* Andre elementer: Spor af andre elementer kan være til stede afhængigt af fremstillingsprocessen.
Konklusion:
* Kemisk renhed: Calciumoxid er kemisk rent, hvilket betyder, at det ideelt set kun består af calcium- og oxygenatomer.
* Praktisk renhed: Den praktiske renhed af calciumoxid varierer afhængigt af dets kilde og håndtering. Det kan indeholde urenheder, selvom de er i små mængder.
Selvom calciumoxid er kemisk rent, kan dets praktiske renhed derfor påvirkes af faktorer som fugtabsorption og reaktioner med den omgivende atmosfære.
 Varme artikler
Varme artikler
-
 Kemikalier, der almindeligvis anvendes i High School Chemistry LabsAf Julia Barrus Opdateret 30. august 2022 Kemi er © Milosz1 (Mi?osz) under Creative Commons Attribution-licensen. Kemilaboratorier på gymnasier arbejder med de samme kernekemikalier som professione
Kemikalier, der almindeligvis anvendes i High School Chemistry LabsAf Julia Barrus Opdateret 30. august 2022 Kemi er © Milosz1 (Mi?osz) under Creative Commons Attribution-licensen. Kemilaboratorier på gymnasier arbejder med de samme kernekemikalier som professione -
 Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt
Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt -
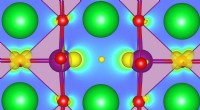 Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse
Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse -
 Video:Hvorfor smider vi gødning på skovbrande?Kredit:The American Chemical Society Når skovbrande udbryder på varme, blæsende dage, de udgør en alvorlig trussel mod mennesker og miljø. Denne uge om reaktioner, Lær, hvordan brandmænd bruger g
Video:Hvorfor smider vi gødning på skovbrande?Kredit:The American Chemical Society Når skovbrande udbryder på varme, blæsende dage, de udgør en alvorlig trussel mod mennesker og miljø. Denne uge om reaktioner, Lær, hvordan brandmænd bruger g


