Forståelse af polære kovalente bindinger:Ulige elektrondeling
Her er hvorfor:
* Kovalente bindinger involverer deling af elektroner mellem atomer.
* Polære kovalente bindinger opstår, når atomerne involveret i bindingen har forskellige elektronegativiteter. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding.
* Atomet med den højere elektronegativitet vil trække de delte elektroner tættere på sig selv og skabe en delvis negativ ladning (δ-) på det atom og en delvis positiv ladning (δ+) på det andet atom.
* Denne ujævne deling af elektroner resulterer i et dipolmoment , hvor den ene ende af molekylet har en let negativ ladning og den anden ende har en let positiv ladning.
Eksempler på polære kovalente bindinger:
* Bindingen mellem brint og oxygen i vand (H2O). Ilt er mere elektronegativt end brint, så elektronerne trækkes tættere på iltatomet, hvilket gør det lidt negativt og brintatomerne lidt positive.
* Bindingen mellem kulstof og oxygen i kuldioxid (CO₂). Ilt er mere elektronegativt end kulstof, hvilket skaber en polær kovalent binding.
Sig til, hvis du har andre spørgsmål!
Sidste artikelKationer vs. forældreatomer:Forstå størrelsesforskelle
Næste artikelBeregn massen af methanol:en trin-for-trin guide
 Varme artikler
Varme artikler
-
 Hackmanite ændrer også farve ved udsættelse for nuklear stråling:Hukommelsessporing muliggør ny…Hackmanitplader, der har skiftet farve ved stråling i laboratoriet hos den finske strålings- og nuklearsikkerhedsmyndighed. Pladerne viser den uddybende farve, efterhånden som stråledosis øges:Jo kort
Hackmanite ændrer også farve ved udsættelse for nuklear stråling:Hukommelsessporing muliggør ny…Hackmanitplader, der har skiftet farve ved stråling i laboratoriet hos den finske strålings- og nuklearsikkerhedsmyndighed. Pladerne viser den uddybende farve, efterhånden som stråledosis øges:Jo kort -
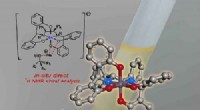 Galliumbaseret opløsningsmiddel analyserer effektivt optisk aktive alkoholerFigur:Skematisk afbildning af in-situ direkte 1H NMR chiral analyse. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Et KAIST-forskerhold har udviklet et galliumbaseret metalkomp
Galliumbaseret opløsningsmiddel analyserer effektivt optisk aktive alkoholerFigur:Skematisk afbildning af in-situ direkte 1H NMR chiral analyse. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Et KAIST-forskerhold har udviklet et galliumbaseret metalkomp -
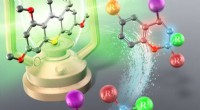 Lad der være lys:Syntetisering af organiske forbindelserBilledet illustrerer den grønt-lys-drevne produktion af oxygen-heterocykler. Kredit:Yokohama National University Enhver biologisk reaktion er en kemisk reaktion. Udveksling af kuldioxid med ilt i
Lad der være lys:Syntetisering af organiske forbindelserBilledet illustrerer den grønt-lys-drevne produktion af oxygen-heterocykler. Kredit:Yokohama National University Enhver biologisk reaktion er en kemisk reaktion. Udveksling af kuldioxid med ilt i -
 Kulstofopsamlingsteknologi skrubber CO2 fra kraftværker som dykkerudstyrCO2 frigives ved mild opvarmning af det faste BIG-bicarbonat. Den frigivne CO2-gas er fanget i den orange ballon, mens de frigjorte vanddampe fanges af kondens i det isafkølede U-formede rør. Kredit:N
Kulstofopsamlingsteknologi skrubber CO2 fra kraftværker som dykkerudstyrCO2 frigives ved mild opvarmning af det faste BIG-bicarbonat. Den frigivne CO2-gas er fanget i den orange ballon, mens de frigjorte vanddampe fanges af kondens i det isafkølede U-formede rør. Kredit:N
- Hvilket udtryk beskriver de forandringer, som en organisme gennemgår?
- Maskinlæring hjælper forudsigelse af jordskælvsrisiko
- Beskyttelse af Artemis og måneforskere mod rumstråling
- GPM -satellit finder kraftig nedbør på den nordlige side af tyfonen Lingling
- Hvad kaldes en hævet jordstrimmel?
- Børn, der spiser frokost, scorer 18 procent højere i læsetest, viser ny undersøgelse


