Forståelse af salte af svage syrer og baser:Hydrolyse og pH
Her er en oversigt:
Karakteristika for salte af svage syrer og baser:
* Hydrolyse: Disse salte reagerer med vand, hvilket får opløsningens pH til at afvige fra neutral.
* pH afhængig af styrken af syren og basen: Opløsningens pH vil afhænge af, om syren eller basen er stærkere.
* Hvis den svage syre er stærkere end den svage base, vil opløsningen være sur.
* Hvis den svage base er stærkere end den svage syre, vil opløsningen være basisk.
* Hvis syren og basen har lignende styrker, vil opløsningen være omtrent neutral.
* Bufferkapacitet: Nogle salte af svage syrer og baser kan fungere som buffere, hvilket betyder, at de kan modstå ændringer i pH, når små mængder syre eller base tilsættes. Dette skyldes, at saltet og dets hydrolyseprodukter danner en ligevægt, der kan absorbere tilsatte H+ eller OH- ioner.
Eksempler:
* Ammoniumacetat (NH4CH3COO): Dette er et salt dannet af den svage syre eddikesyre (CH3COOH) og den svage base ammoniak (NH3). Opløsningen vil være let sur, fordi eddikesyre er en stærkere syre end ammoniak er en base.
* Natriumcarbonat (Na2CO3): Dette er et salt dannet af den svage syre kulsyre (H2CO3) og den stærke base natriumhydroxid (NaOH). Opløsningen vil være basisk, fordi natriumhydroxid er en stærkere base, end kulsyre er en syre.
Forståelse af hydrolyse:
Hydrolysereaktionen for et salt af en svag syre og en svag base involverer saltioner, der reagerer med vandmolekyler for at danne den svage syre og svage base igen. For eksempel kan hydrolysen af ammoniumacetat repræsenteres som:
NH4+ (aq) + H2O(l) ⇌ NH3(aq) + H3O+ (aq)
CH3COO- (aq) + H2O(l) ⇌ CH3COOH(aq) + OH- (aq)
Dannelsen af H3O+ (hydroniumioner) gør opløsningen let sur.
Opsummering:
Salte af svage syrer og svage baser kan forstås gennem deres hydrolysereaktioner, som påvirker opløsningens pH baseret på de relative styrker af syren og basen. Disse salte kan også bidrage til buffereffekter i opløsninger.
 Varme artikler
Varme artikler
-
 Hvordan metalatomer kan arrangere sig på en isolatorKredit:CC0 Public Domain For at producere bittesmå elektroniske hukommelser eller sensorer i fremtiden, det er vigtigt at kunne arrangere individuelle metalatomer på et isolerende lag. Forskere ve
Hvordan metalatomer kan arrangere sig på en isolatorKredit:CC0 Public Domain For at producere bittesmå elektroniske hukommelser eller sensorer i fremtiden, det er vigtigt at kunne arrangere individuelle metalatomer på et isolerende lag. Forskere ve -
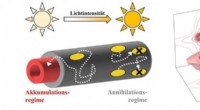 Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff
Energiflow i nanoområdetKredit:Billeder:Björn Kriete (v.) / Stefan Mueller (r.) Planter og bakterier kan fange sollysets energi med lys-høstende antenner og overføre den til et reaktionscenter. At transportere energi eff -
 Bioingeniører udvikler sig hurtigt, spyt-baseret detektionstest for marihuanaKredit:University of Texas i Dallas Dr. Shalini Prasad (forrest), midlertidig afdelingsleder for bioingeniør ved Erik Jonsson School of Engineering and Computer Science, har den THC-biosensor, som
Bioingeniører udvikler sig hurtigt, spyt-baseret detektionstest for marihuanaKredit:University of Texas i Dallas Dr. Shalini Prasad (forrest), midlertidig afdelingsleder for bioingeniør ved Erik Jonsson School of Engineering and Computer Science, har den THC-biosensor, som -
 Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2
Forskere finder lovende nanopartikelkandidater til kuldioxidopsamling og omdannelseOriginalt kunstværk fra University of Pittsburgh, der viser en kobberbaseret bimetallisk nanopartikel designet til at adsorbere og aktivere kuldioxid, dukkede op på forsiden af ChemSusChem i april 2
- Hvorfor er friktion nyttig kraft?
- Hvilke to ressourcer, der kommer fra atmosfæren og beskriver, hvordan hver bruges?
- Neutronundersøgelse af glaukomlægemidler giver fingerpeg om enzymmål for aggressive kræftformer
- Fem temaer for geografi i Honduras?
- Hvad er 375 F i celsius?
- Hvordan former konkurrencen et økosystem?


