Hvorfor N3H ikke eksisterer:Forståelse af oxidationstilstande
* Nitrogens typiske oxidationstilstande: Nitrogen har almindeligvis oxidationstilstande fra -3 til +5.
* Brints typiske oxidationstilstand: Hydrogen har typisk en oxidationstilstand på +1 (undtagen i metalhydrider, hvor den er -1).
For at afbalancere ladningerne i et molekyle skal summen af alle atomernes oxidationstilstande være lig med nul. Det er umuligt at opnå dette med N3H.
Her er grunden:
* Hvis vi antager, at nitrogen er i sin mest negative tilstand (-3), ville vi have brug for 3 brintatomer (+1 hver) for at balancere det. Dette ville give os NH3 (ammoniak), ikke N3H.
* Hvis nitrogen er i en mindre negativ tilstand, ville vi have brug for endnu flere brintatomer for at balancere ladningen, hvilket afviger yderligere fra N3H-formlen.
Derfor er N3H ikke en stabil forbindelse, og vi kan ikke tildele oxidationsnumre til dets atomer.
 Varme artikler
Varme artikler
-
 Isolerende mursten med mikroskopiske boblerFor at opnå de samme isoleringsværdier som en 165 mm tyk væg af aerobricks, en mur af perlitsten skal være 263 mm tyk — og en mur af ikke-isolerende mursten skal være mere end en meter. Kredit:Empa
Isolerende mursten med mikroskopiske boblerFor at opnå de samme isoleringsværdier som en 165 mm tyk væg af aerobricks, en mur af perlitsten skal være 263 mm tyk — og en mur af ikke-isolerende mursten skal være mere end en meter. Kredit:Empa -
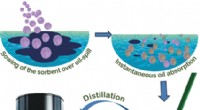 Et organogelator-cellulose-kompositmateriale til praktisk og miljøvenlig genopretning af marine oli…Kredit:Wiley Spildt råolie har gentagne gange forurenet og endda ødelagt marine økosystemer. En effektiv foranstaltning ville være at fjerne spildte oliepletter ved absorption i en adskillelig fas
Et organogelator-cellulose-kompositmateriale til praktisk og miljøvenlig genopretning af marine oli…Kredit:Wiley Spildt råolie har gentagne gange forurenet og endda ødelagt marine økosystemer. En effektiv foranstaltning ville være at fjerne spildte oliepletter ved absorption i en adskillelig fas -
 Afdække hemmelighederne bag gammel klippekunst ved hjælp af røntgensynEt bærbart røntgenapparat har afsløret ny indsigt om de pigmenter, der bruges i klippekunst uden at beskadige stedet. Kredit:Shumla Archaeological Research and Education Center Forhistoriske klipp
Afdække hemmelighederne bag gammel klippekunst ved hjælp af røntgensynEt bærbart røntgenapparat har afsløret ny indsigt om de pigmenter, der bruges i klippekunst uden at beskadige stedet. Kredit:Shumla Archaeological Research and Education Center Forhistoriske klipp -
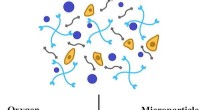 Forskere udvikler fluorescerende sensorer til at spore næringsstoffer i hydrogel-baseret helbredels…Rice Universitys bioingeniører udviklede fluorescerende mikropartikler, der kan suspenderes i hydrogelstilladser, der er podet med levende celler. Mikropartiklerne kan bruges til at overvåge tilstedev
Forskere udvikler fluorescerende sensorer til at spore næringsstoffer i hydrogel-baseret helbredels…Rice Universitys bioingeniører udviklede fluorescerende mikropartikler, der kan suspenderes i hydrogelstilladser, der er podet med levende celler. Mikropartiklerne kan bruges til at overvåge tilstedev
- Tør sommer 2018:En tiendedel af de centraleuropæiske skove mistede blade for tidligt
- Hvad er de to 2 trækkræfter?
- Et objekt, der har en temperatur på 300 K, ville blive bedst observeret med et teleskop?
- Er det ældste rock -lag i bunden?
- Polar is, atmosfærisk vanddamp største drivkraft for variation blandt klimamodeller
- For den varmeste planet, en stor nedsmeltning, viser undersøgelse


