Forståelse af atomer i magnesium (Mg):En omfattende vejledning
* "Mg" refererer til grundstoffet magnesium. Magnesium er et enkelt grundstof, og det består af mange atomer. Vi kan ikke sige, hvor mange atomer der er i "Mg", fordi det er ligesom at spørge, hvor mange æbler der er i ordet "æble".
* "Mg" kunne referere til en specifik prøve af magnesium. For at vide, hvor mange atomer der er i en prøve, skal du kende prøvens masse og bruge Avogadros tal. Sådan gør du:
* Find den molære masse af magnesium: Den molære masse af magnesium er 24,305 g/mol. Det betyder, at et mol magnesiumatomer vejer 24.305 gram.
* Bestem massen af din prøve. Lad os sige, at du har en prøve på 1 gram magnesium.
* Beregn antallet af mol: Divider massen af din prøve med den molære masse:(1 gram) / (24,305 g/mol) =0,0412 mol.
* Brug Avogadros nummer: Avogadros tal fortæller os, at der er 6.022 x 10^23 atomer i et mol af ethvert stof. Gang antallet af mol med Avogadros tal for at få antallet af atomer:(0,0412 mol) * (6,022 x 10^23 atomer/mol) =2,48 x 10^22 atomer.
For at besvare spørgsmålet præcist skal vi derfor kende massen af den prøve af magnesium, du henviser til.
 Varme artikler
Varme artikler
-
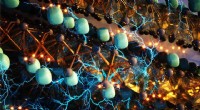 Undersøgelse finder fluor som mulig erstatning for lithium i genopladelige batterierHer, lagdelte elektroder, såsom Ca2N og Y2C - der har en elektron, der optager et gittersted - forudsiges som lovende værter for fluorid-interkalation, fordi deres anioniske elektroner skaber store me
Undersøgelse finder fluor som mulig erstatning for lithium i genopladelige batterierHer, lagdelte elektroder, såsom Ca2N og Y2C - der har en elektron, der optager et gittersted - forudsiges som lovende værter for fluorid-interkalation, fordi deres anioniske elektroner skaber store me -
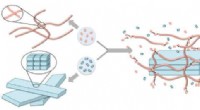 Molekylært stillads hjælper konstruktion på nanoskalaKredit:Okinawa Institute of Science and Technology Graduate University Hvis du vil bygge et højt hus, du skal bruge stillads. Professor Ye Zhang og kolleger ved Okinawa Institute of Science and Te
Molekylært stillads hjælper konstruktion på nanoskalaKredit:Okinawa Institute of Science and Technology Graduate University Hvis du vil bygge et højt hus, du skal bruge stillads. Professor Ye Zhang og kolleger ved Okinawa Institute of Science and Te -
 Forøgelse af løsningsmolaritet:Gennemprøvede teknikker og praktiske tipsAf Matthew Perdue Opdateret 24. marts 2022 En opløsning er en blanding af to dele:et opløst stof og et opløsningsmiddel. Det opløste stof er den opløste partikel i opløsningen, og opløsningsmidlet
Forøgelse af løsningsmolaritet:Gennemprøvede teknikker og praktiske tipsAf Matthew Perdue Opdateret 24. marts 2022 En opløsning er en blanding af to dele:et opløst stof og et opløsningsmiddel. Det opløste stof er den opløste partikel i opløsningen, og opløsningsmidlet -
 Forskere omdanner ultrahård pollen til fleksibelt materialeDette pollen-afledte materiale har potentialet til at fungere som en byggesten til design af nye kategorier af miljøvenlige materialer. Afbildet i forgrunden:svampe og papir afledt af pollen. Kredit:N
Forskere omdanner ultrahård pollen til fleksibelt materialeDette pollen-afledte materiale har potentialet til at fungere som en byggesten til design af nye kategorier af miljøvenlige materialer. Afbildet i forgrunden:svampe og papir afledt af pollen. Kredit:N
- En dobbelt kovalent kemisk binding repræsenterer delingen af hvor mange valg?
- Forskere revolutionerer solenergi med ny guld nanokluster teknologi
- Hvordan politiets body cam-videoer påvirker nævninge anderledes end dashcam-videoer
- Stjerner for gamle til at stole på? En mulig stjerneløsning det kosmologiske lithiumproblem
- Hvordan vinder du en nobelpris?
- Smartphonen:et globalt produkt


