Forøgelse af løsningsmolaritet:Gennemprøvede teknikker og praktiske tips
Af Matthew Perdue Opdateret 24. marts 2022
En opløsning er en blanding af to dele:et opløst stof og et opløsningsmiddel. Det opløste stof er den opløste partikel i opløsningen, og opløsningsmidlet er den del, der opløser det opløste stof. For eksempel er saltvand en opløsning sammensat af natriumchlorid, det opløste stof, opløst i vand, opløsningsmidlet. Molaritet er en måling, der bruges til at identificere mængden af opløst stof, i mol, opløst i et opløsningsmiddel efter volumen og udtrykkes som mol pr. liter (mol/L). Molariteten er derfor direkte proportional med mængden af opløst stof i opløsning og indirekte proportional med opløsningens volumen. Disse to forhold kan bruges til at bestemme, hvordan man kan øge molariteten af enhver opløsning.
Forøgelse af molariteten efter volumen
Trin 1
Bestem antallet af mol opløst stof i en given opløsning ved at dividere antallet af gram opløst stof med dets molekylvægt. For eksempel ville en saltvandsopløsning indeholdende 5 gram natriumchlorid have 0,18 mol som bestemt ved at dividere mængden af opløst stof, i gram, med dets molekylvægt (5 g / 28 g/mol =0,18 mol opløst stof).
Trin 2
Anbring opløsningen i et målebæger, og identificer opløsningens volumen. De fleste bægerglas har mål markeret i milliliter. Da molariteten er angivet i liter, skal volumen i milliliter omregnes til liter ved at gange med omregningsfaktoren 1 L / 1000 mL. Ved at bruge saltvandseksemplet ville et målt volumen på 150 mL svare til 0,15 L ved hjælp af konverteringsfaktoren:150 mL x (1 L / 1000 mL) =0,15 L.
Trin 3
Identificer molariteten (M) af opløsningen baseret på de beregnede mol opløst stof og observeret volumen i milliliter. Molariteten af saltvandsopløsningen ville være 0,18 mol opløst stof pr. 0,15 L. eller 1,2 M, fordi 0,18 mol / 0,15 L =1,2 mol/L.
Trin 4
Bestem den ændring i volumen, der kræves for at øge molariteten til en specificeret værdi ved hjælp af ligningen M1 x V1 =M2 x V2, hvor M1 og M2 er de initiale og nye molariteter, og V1 og V2 er henholdsvis initial- og slutvolumen. En fordobling af molariteten af eksempelsaltvandsopløsningen fra 1,2 til 2,4 ville kræve et nyt volumen på 0,08 L som bestemt ved at løse for V2 i ligningen 1,2 M x 0,15 L =2,4 M x V2.
Trin 5
Lav den nye opløsning ved at bruge den samme mængde opløst stof og nyberegnet volumen opløsningsmiddel. Den nye saltvandsopløsning ville stadig indeholde 5 g natriumchlorid, men kun 0,075 L, eller 75 ml, vand for at resultere i en ny opløsning med en molaritet på 2,4. Derfor resulterer et fald i volumen af en opløsning med den samme mængde opløst stof i en stigning i molariteten.
Forøg molariteten med opløst stof
Trin 1
Bestem molariteten af en bestemt opløsning ved at følge trin 1 til 3 i det foregående afsnit.
Trin 2
Identificer den ønskede stigning i molaritet for opløsningen. Antag for eksempel, at en indledende 1,2 M opløsning af saltvand skal øges til en 2,4 M opløsning med samme volumen.
Trin 3
Bestem, hvor meget opløst stof der skal tilsættes til opløsningen for at øge molariteten til den specificerede værdi. En 2,4 M opløsning ville indeholde 2,4 mol pr. liter, og opløsningen indeholder 0,15 L. Mængden af opløst stof, i mol, af den nye opløsning identificeres derefter ved at opsætte et forhold givet som 2,4 mol/ 1 L =x mol / 0,15 L og løse for den ukendte x-værdi. Denne beregning identificerer en værdi på 0,36 mol natriumchlorid, der kræves til den nye opløsning. Hvis man multiplicerer med molekylmassen af natriumchlorid (28 g/mol), får man den nødvendige mængde i gram opløst stof som 10,1 g.
Trin 4
Træk den oprindelige mængde opløst stof fra den nyligt beregnede mængde for at bestemme mængden af opløst stof, der skal tilsættes for at øge molariteten. For at øge en 1,2 M saltvandsopløsning med 5 gram natriumchlorid til en 2,4 M opløsning kræver tilsætning af 5,1 gram natriumchlorid som bestemt ved at trække den indledende mængde på 5 g fra den nyligt nødvendige mængde på 10,1 g. Derfor ville tilsætning af 5,1 g natriumchlorid til en 1,2 M saltvandsopløsning øge molariteten til 2,4 M.
Ting påkrævet
- Klassificeret bægerglas
- Periodisk tabel
- Lommeregner
- Natriumchlorid
- Vand
 Varme artikler
Varme artikler
-
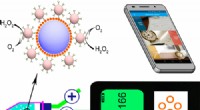 Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr
Nye sensorer kan muliggøre en mere overkommelig påvisning af forurening og sygdommeKredit:American Chemical Society Når det kommer til at teste for kræft, miljøforurening og fødevareforurenende stoffer, traditionelle sensorer kan hjælpe. Udfordringerne er, at de ofte er omfangsr -
 En ny måde at fjerne generende ioner fra vandKredit:Wageningen Universitet At omdanne havvand til ferskvand er vigtigt i lande med knaphed på vand. Til den proces, visse ladede partikler - kendt som ioner - skal fjernes fra vandet. Imidlerti
En ny måde at fjerne generende ioner fra vandKredit:Wageningen Universitet At omdanne havvand til ferskvand er vigtigt i lande med knaphed på vand. Til den proces, visse ladede partikler - kendt som ioner - skal fjernes fra vandet. Imidlerti -
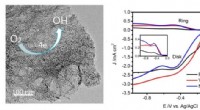 Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare
Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare -
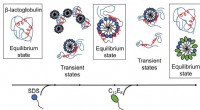 Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss
Fanget i sæbehånd:At forstå, hvordan sæbemolekyler hjælper proteiner med at komme ind og ud af …Resultater offentliggjort af AU-forskere afslører, at surfaktant-medieret udfoldning og genfoldning af proteiner er komplekse processer med flere strukturer til stede, og omarrangeringer sker på tidss
- Smelter syren i citroner plastikkopper?
- Hvor mange kopper i 9,47 ounces?
- Hvad er mængden af energi, der bæres af en foton, der har frekvens 5,71x1014Hz?
- Råoliesammensætning:Forståelse af kulbrinteblandinger
- Hvorfor er velhavende forbrugere mindre tilbøjelige til at købe luksusvarer under en recession?
- Hvad er forholdet mellem kromosomer og DNA -molekyler?


