Trin-for-trin guide til fremstilling af nøjagtige fortyndingsopløsninger
Af Regina Edwards, Opdateret 24. marts 2022
Yanawut/iStock/GettyImages
En fortyndingsopløsning er en blanding af et koncentreret "stamstof" og et neutraliserende "fortynder". Forholdet mellem de to bestemmer den endelige koncentration. For eksempel betyder en 1:10 fortynding, at 10 ml af den endelige blanding indeholder 1 ml stamopløsning og 9 ml fortyndingsmiddel. Den følgende metode viser, hvordan man beregner de nøjagtige mængder, der er nødvendige for enhver fortyndingsfaktor. Denne tilgang følger standard laboratoriepraksis, der i vid udstrækning anvendes i akademiske og industrielle omgivelser.
Trin 1:Definer det endelige volumen
Beslut hvor meget totalløsning du har brug for. For eksempel 30mL.
Trin 2:Angiv fortyndingsforholdet
Skriv forholdet som et forhold, f.eks. 1:20 (en del lager til tyve dele i alt).
Trin 3:Konverter til en brøk
Udtryk forholdet som en brøk:1 ÷ 20 =1/20.
Trin 4:Beregn lagervolumen
Multiplicer det ønskede slutvolumen med fraktionen:30mL × 1/20 =1,5mL lager.
Trin 5:Bestem fortyndingsvolumen
Træk stamvolumenet fra totalen:30mL – 1,5mL =28,5mL fortynder.
Trin 6:Mål beholdningen
Brug en målecylinder til at trække 1,5 ml af stamopløsningen i en ren beholder.
Trin 7:Mål fortyndingsmidlet
Mål 28,5 ml af fortyndingsmidlet (f.eks. vand eller opløsningsmiddel), og tilsæt det til den samme beholder.
Trin 8:Bland grundigt
Rør den kombinerede opløsning med en glasstang, indtil den er homogen. Din 1:20-fortynding er klar.
Nødvendige materialer
- Skåren cylinder (eller pipette) til nøjagtig volumenmåling
- Rengør målebæger eller hætteglas
- Rørestav af glas
- Videnskabelig lommeregner eller regneark til hurtig aritmetik
Nøjagtige fortyndingsberegninger er afgørende for reproducerbare eksperimenter og pålidelige data.
 Varme artikler
Varme artikler
-
 Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl
Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl -
 Lyser vejen til porøs elektronik og sensorerFig.1 Nanostruktur porøs titaniumoxid tynd film (TiOx) aflejret på plast (PI:polyimid) substratet. Kredit:Osaka University Mange almindelige husholdningsartikler og enheder har en belægning, der f
Lyser vejen til porøs elektronik og sensorerFig.1 Nanostruktur porøs titaniumoxid tynd film (TiOx) aflejret på plast (PI:polyimid) substratet. Kredit:Osaka University Mange almindelige husholdningsartikler og enheder har en belægning, der f -
 At forstå atomer:protoner, neutroner, elektroner og deres rollerAf Kevin Beck Opdateret 30. august 2022 Creatas/Creatas/Getty Images Atomet, afledt af det græske ord, der betyder det, der ikke kan opdeles, er den grundlæggende enhed i alt stof. Det er sammensat
At forstå atomer:protoner, neutroner, elektroner og deres rollerAf Kevin Beck Opdateret 30. august 2022 Creatas/Creatas/Getty Images Atomet, afledt af det græske ord, der betyder det, der ikke kan opdeles, er den grundlæggende enhed i alt stof. Det er sammensat -
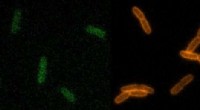 Forskning går fremad med søgning efter nye antibiotikaCellevæggene i levende bakterier lyser grønt, orange og rød med tre forskellige typer RfDAA -prober. Kredit:VanNieuwenhze Lab, Indiana University Indiana University forskere fremmer viden om, hvor
Forskning går fremad med søgning efter nye antibiotikaCellevæggene i levende bakterier lyser grønt, orange og rød med tre forskellige typer RfDAA -prober. Kredit:VanNieuwenhze Lab, Indiana University Indiana University forskere fremmer viden om, hvor
- Klimaændringer som katalysator i Greater Cahokia
- Udforskning af omdannelsen af varme til elektricitet i enkelte molekyler
- Hvilken specifik struktur indeholder chlorophyll?
- Er planetrotation en videnskabsrapport eller eksperiment?
- Hvilke hapens til densiteten, hvis både volumen og masse er fordoblet?
- Hvilken teori om pladebevægelse er afhængig af den vægtsubducerende skorpe?


