Ioner vs. elektrolytter:Forståelse af deres roller i biologi og industri
Af Michael Judge
Opdateret 24. marts 2022
ioner
I kemi er en ion en ladet art, der dannes, når et atom eller en gruppe af atomer mister eller får elektroner. Mens et neutralt atom indeholder lige mange protoner (positivt ladede) og elektroner (negativt ladede), giver fjernelse eller tilføjelse af en eller flere elektroner en nettoladning. Denne grundlæggende egenskab ligger til grund for utallige biologiske processer – såsom nerveimpulstransmission – og industrielle applikationer som galvanisering.
Elektrolytter
En elektrolyt er enhver forbindelse, der frigiver ioner, når den opløses i vand. Under opløsning brydes de kemiske bindinger i det opløste stof, hvilket skaber fritgående ladede partikler, der stabiliseres af vandmolekylernes let polære natur. Dette fænomen gør det muligt for elektrolytter at lede elektricitet, et princip, der udnyttes i alt fra det menneskelige nervesystem til moderne batterier.
Typer af elektrolytter
Elektrolytter er kategoriseret efter omfanget af deres dissociation i opløsning:
- Stærke elektrolytter dissocierer fuldstændigt og efterlader næsten ingen udissocierede molekyler. Almindelige eksempler omfatter natriumchlorid (NaCl), som producerer Na⁺- og Cl⁻-ioner, og saltsyre (HCl), som giver H⁺ og Cl⁻.
- Svage elektrolytter delvist adskilles, så en betydelig del forbliver intakt. Eddikesyre (CH₃COOH) er en typisk svag elektrolyt, der producerer en begrænset mængde acetat (CH₃COO⁻) og H⁺-ioner.
Elektrolytapplikationer
Ionerne genereret af elektrolytter er essentielle for adskillige funktioner:
- Fysiologiske processer – Den menneskelige krop er afhængig af elektrolytter som NaCl til at opretholde cellulær homeostase, nerveledning og væskebalance.
- Energilager – Batterier bruger elektrolytopløsninger indeholdende ioner såsom Zn²⁺ og Cu²⁺ for at lette ladningsoverførslen mellem elektroderne.
- Industrikemi – Elektrolytter, både sure og basiske, er en integreret del af metalbearbejdning, kemisk syntese og fremstilling af hverdagsprodukter.
 Varme artikler
Varme artikler
-
 Linsefri OLED'er med effektivitet sammenlignelig med uorganiske LED'erFigur 1. Fotografier af OLEDer med SiO2-indlejrede spredningslag i henhold til spredning. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Brugen af organiske lysemitterende dio
Linsefri OLED'er med effektivitet sammenlignelig med uorganiske LED'erFigur 1. Fotografier af OLEDer med SiO2-indlejrede spredningslag i henhold til spredning. Kredit:Korea Advanced Institute of Science and Technology (KAIST) Brugen af organiske lysemitterende dio -
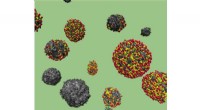 Syntesestudier omdanner affaldssukker til bæredygtige energilagringsapplikationerEn molekylær dynamik-simulering afbilder solide (sort) og hule (flerfarvede) kulstofkugler afledt af affaldssukkerstrømme fra bioraffinaderier. De hule kuglers egenskaber er ideelle til udvikling af e
Syntesestudier omdanner affaldssukker til bæredygtige energilagringsapplikationerEn molekylær dynamik-simulering afbilder solide (sort) og hule (flerfarvede) kulstofkugler afledt af affaldssukkerstrømme fra bioraffinaderier. De hule kuglers egenskaber er ideelle til udvikling af e -
 Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo
Support driver skæbnen for beskyttede guld-nanoklynger som katalysatorerForskningen blev lavet på forsiden af Chemistry-A European Journal i juni 2020. På billedet:guldklynger (gule ædelstene) beskyttet af organiske molekyler (lyserøde og blå ædelstene) opdeles på to fo -
 Stive fibre spundet af slimSlankt jagtvåben:fløjlsorm, der ligner larver med korte ben, fange bytte med en sekretion, der danner polymertråde, mens byttet kæmper for at frigøre sig selv. Kredit:Alexander Bär / Nature Communicat
Stive fibre spundet af slimSlankt jagtvåben:fløjlsorm, der ligner larver med korte ben, fange bytte med en sekretion, der danner polymertråde, mens byttet kæmper for at frigøre sig selv. Kredit:Alexander Bär / Nature Communicat


