Ædelgasser:hvorfor de ikke danner forbindelser og bemærkelsesværdige eksempler
* Helium (han)
* Neon (Ne)
* Argon (Ar)
* Krypton (Kr)
* Xenon (Xe)
* Radon (Rn)
Hvorfor danner ædelgasser ikke forbindelser?
Ædelgasser har en fuld ydre skal af elektroner, hvilket gør dem meget stabile og ikke-reaktive. De har ingen tendens til at vinde, miste eller dele elektroner for at danne kemiske bindinger. Det er derfor, de kaldes "inerte gasser".
Undtagelser:
Selvom ædelgasser generelt ikke er reaktive, er der nogle undtagelser:
* Xenon og krypton kan danne forbindelser med stærkt elektronegative elementer som fluor og oxygen under specifikke forhold.
* Radon er radioaktiv og har en kort halveringstid, så dens reaktivitet er ikke velundersøgt.
Derfor, mens udtrykket "inerte gasser" ikke er helt nøjagtigt, anses ædelgasser stadig for at være de grundstoffer, der normalt ikke danner forbindelser.
 Varme artikler
Varme artikler
-
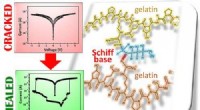 Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater
Selvreparerende gelatinebaseret film kan være et smart træk for elektronikKredit:American Chemical Society At tabe en mobiltelefon kan nogle gange forårsage overfladiske revner. Men andre gange, enheden kan helt stoppe med at fungere, fordi der udvikles brud i det mater -
 En ny måde at kombinere bløde materialer påEn umodificeret hydrogel (til venstre) skræller let af fra en elastomer. En kemisk bundet hydrogel og elastomer (til højre) er svære at skille fra hinanden, efterlader rester efter kredit:Suo Lab/Harv
En ny måde at kombinere bløde materialer påEn umodificeret hydrogel (til venstre) skræller let af fra en elastomer. En kemisk bundet hydrogel og elastomer (til højre) er svære at skille fra hinanden, efterlader rester efter kredit:Suo Lab/Harv -
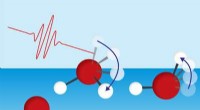 Vandoverflademolekyler mister energi ved rotation af den frie OH -gruppeFigur 1:I modsætning til andre vandmolekyler (røde kugler:oxygenatomer; hvide kugler:brintatomer), dem på overfladen har en fri hydroxylgruppe (OH). Tahei Tahara og hans team har brugt ultrahurtig spe
Vandoverflademolekyler mister energi ved rotation af den frie OH -gruppeFigur 1:I modsætning til andre vandmolekyler (røde kugler:oxygenatomer; hvide kugler:brintatomer), dem på overfladen har en fri hydroxylgruppe (OH). Tahei Tahara og hans team har brugt ultrahurtig spe -
 Grønt alternativ til PET kunne være endnu grønnereProfessor i polymerkemi Katja Loos. Kredit:Universitetet i Groningen En af de mest succesrige plasttyper er polyethylenterephthalat (PET), det materiale, vi bruger til at lave flasker og fibre til
Grønt alternativ til PET kunne være endnu grønnereProfessor i polymerkemi Katja Loos. Kredit:Universitetet i Groningen En af de mest succesrige plasttyper er polyethylenterephthalat (PET), det materiale, vi bruger til at lave flasker og fibre til
- Sådan fremstilles en pladespiller til et Kids Science Project
- Hvad er modstanden for luft til et bevægende objekt?
- Hvilken tilstand af stof er argon ved 25 grader celsius?
- En primær standard for måling af vakuum
- New Horizons rumfartøj tager den indvendige kurs til Ultima Thule
- Mudslides, oversvømmelse og lavine advarsler - Hvorfor Californien havde sådan en våd vejr uge


