Vands amfotere natur:Forståelse af syre-base-adfærd
Sådan fungerer det:
* Vand som en syre: Vand kan donere en proton (H+) for at danne hydroxidionen (OH-). Dette sker, når vand reagerer med en base.
* Eksempel:HCl (syre) + H₂O (base) → H₃O+ (hydroniumion) + Cl-
* Vand som base: Vand kan acceptere en proton (H+) for at danne hydroniumionen (H₃O+). Dette sker, når vand reagerer med en syre.
* Eksempel:NH₃ (base) + H₂O (syre) → NH4+ (ammoniumion) + OH-
Vands evne til at fungere som både en syre og en base gør det muligt for det at deltage i reaktioner, der producerer syrer og baser.
Opsummering:
Vandets amfotere natur, dets evne til både at donere og acceptere protoner, er nøglen til dets rolle i syre-base kemi.
Sidste artikelStærk syreionisering i vand:En komplet forklaring
Næste artikelForståelse af syrer:definition, egenskaber og karakteristika
 Varme artikler
Varme artikler
-
 Edderkoppesilke fremstillet af fotosyntetiske bakterierEdderkopper producerer utroligt stærke og lette tråde lavet af silkeproteiner, som kan bruges til fremstilling af nyttige materialer. Det lykkedes for forskere at fremstille edderkoppesilken ved hjælp
Edderkoppesilke fremstillet af fotosyntetiske bakterierEdderkopper producerer utroligt stærke og lette tråde lavet af silkeproteiner, som kan bruges til fremstilling af nyttige materialer. Det lykkedes for forskere at fremstille edderkoppesilken ved hjælp -
 Ny krydsfænomenteori kunne forudsige effektiviteten af nye materialerVarme fra Solen resulterer i forskellige eksempler på krydsfænomener såsom fordampning af vand og fotosyntese til vækst af træer og afgrøder. Kredit:Elizabeth Flores-Gomez Murray. Alle rettigheder for
Ny krydsfænomenteori kunne forudsige effektiviteten af nye materialerVarme fra Solen resulterer i forskellige eksempler på krydsfænomener såsom fordampning af vand og fotosyntese til vækst af træer og afgrøder. Kredit:Elizabeth Flores-Gomez Murray. Alle rettigheder for -
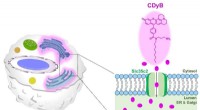 En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi
En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi -
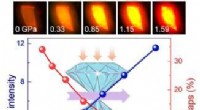 Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research
Tryk undertrykker bærerindfangning i 2-D halogenidperovskitFluorescensmikrografer under kompression og PL-intensiteten og bidraget fra de fangede staters emission som funktion af tryk. Kredit:Center for High Pressure Science &Technology Advanced Research


