Betydningen af brintbindinger i vands egenskaber
1. Højt kogepunkt og smeltepunkt:
* Hydrogenbindinger kræver betydelig energi for at bryde, hvilket bidrager til vands relativt høje kogepunkt (100°C) og smeltepunkt (0°C). Dette muliggør eksistensen af flydende vand over en lang række temperaturer, som er afgørende for livet.
2. Høj overfladespænding:
* Hydrogenbindinger skaber en stærk sammenhængskraft mellem vandmolekyler, hvilket resulterer i høj overfladespænding. Dette gør det muligt for insekter at gå på vandet og gør det muligt for vandet at danne dråber.
3. Fremragende opløsningsmiddel:
* Vands polære natur, lettet af hydrogenbinding, gør det muligt for det at opløse en lang række stoffer, herunder salte, sukkerarter og gasser. Dette gør vand til et fremragende opløsningsmiddel til biologiske reaktioner og næringsstoftransport.
4. Varmekapacitet:
* Vand har en høj varmekapacitet, hvilket betyder, at det kan absorbere en stor mængde varme, før dets temperatur stiger markant. Dette hjælper med at regulere temperaturudsving i organismer og miljøer.
5. Densitetsanomali:
* Vand er tættest ved 4°C. Over og under denne temperatur bliver vandet mindre tæt. Denne anomali giver mulighed for dannelse af is på overfladen af vandområder, hvilket giver isolering og gør det muligt for vandlevende liv at overleve.
6. Transport:
* Vand fungerer som et transportmedium for næringsstoffer, gasser og affaldsprodukter i organismer. Dette lettes af dets evne til at opløse forskellige stoffer og dets sammenhængende natur.
7. Biomolekylestruktur og funktion:
* Hydrogenbindinger er afgørende for at opretholde strukturen og funktionen af biologiske molekyler som proteiner, nukleinsyrer (DNA og RNA) og kulhydrater.
Opsummering, hydrogenbinding spiller en afgørende rolle i at gøre vand til et ideelt opløsningsmiddel, lette temperaturregulering og understøtte liv på Jorden. Disse egenskaber er afgørende for at opretholde det kemiske og fysiske miljø, der kræves for livsprocesser.
 Varme artikler
Varme artikler
-
 Beregning af teoretisk udbytte:En praktisk vejledning for kemikereAf Kaylee Finn, Opdateret 30. august 2022 Vicheslav/iStock/GettyImages Teoretisk udbytte er et grundlæggende begreb i kemi, der repræsenterer den maksimale mængde produkt, der kan dannes, når en rea
Beregning af teoretisk udbytte:En praktisk vejledning for kemikereAf Kaylee Finn, Opdateret 30. august 2022 Vicheslav/iStock/GettyImages Teoretisk udbytte er et grundlæggende begreb i kemi, der repræsenterer den maksimale mængde produkt, der kan dannes, når en rea -
 En meget alkalisk stabil Co3O4@Co-MOF-komposit til højtydende elektrokemisk energilagringEt søjlediagram til sammenligning af kapacitansydelse af elektrodematerialer. Kredit:©Science China Press Metal-organiske rammer (MOFer) dannes via selvsamling af metalioner og organiske linkere.
En meget alkalisk stabil Co3O4@Co-MOF-komposit til højtydende elektrokemisk energilagringEt søjlediagram til sammenligning af kapacitansydelse af elektrodematerialer. Kredit:©Science China Press Metal-organiske rammer (MOFer) dannes via selvsamling af metalioner og organiske linkere. -
 Videnskaben bag vandfrysning:Fra molekyler til isudvidelseAf Ann Johnson, Opdateret 24. marts 2022 Molekylær bevægelse under frysning Når vand skifter fra flydende til fast stof, går dets molekyler fra en konstant, kaotisk dans til et højt ordnet gitter. I
Videnskaben bag vandfrysning:Fra molekyler til isudvidelseAf Ann Johnson, Opdateret 24. marts 2022 Molekylær bevægelse under frysning Når vand skifter fra flydende til fast stof, går dets molekyler fra en konstant, kaotisk dans til et højt ordnet gitter. I -
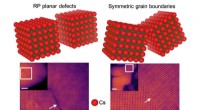 Når en defekt kan være gavnligVed hjælp af atomopløsningselektronmikroskopi, Arashdeep Singh Thind, en kandidatstuderende i Rohan Mishras laboratorium, studeret korngrænser i krystaller (se pile). Kredit:Washington University i St
Når en defekt kan være gavnligVed hjælp af atomopløsningselektronmikroskopi, Arashdeep Singh Thind, en kandidatstuderende i Rohan Mishras laboratorium, studeret korngrænser i krystaller (se pile). Kredit:Washington University i St
- Hastighed er et mål for en genstande, hvilke to ting?
- Hvad er breddegrad og længdegrad af Mount Nevado del Ruiz?
- Hvilke data observeres gennem vores sanser?
- Hvad er verdens korteste flod?
- Sporing af udviklingen af bregners overraskende sød forsvarsstrategi
- Hvad var det første højdrevne observatorium placeret i rummet kaldet?


