Videnskaben bag vandfrysning:Fra molekyler til isudvidelse
Af Ann Johnson, Opdateret 24. marts 2022
Molekylær bevægelse under frysning
Når vand skifter fra flydende til fast stof, går dets molekyler fra en konstant, kaotisk dans til et højt ordnet gitter. I flydende tilstand kolliderer molekyler, glider forbi hinanden og bliver aldrig på det samme sted længe. Når temperaturen falder til 32°F (0°C), sænkes bevægelsen, og molekylerne låser sig fast i et gentaget, krystallinsk arrangement, som vi ser som is.
Molekylær tiltrækning og frysepunktet
Hvert molekyle oplever kræfter, der trækker det mod dets naboer. Stærke attraktioner, som dem i kulstof, kan holde atomer sammen selv ved tusindvis af grader, mens svage kræfter i helium betyder, at det forbliver gasformigt indtil ekstrem kulde. Vands intermolekylære kræfter er moderate - stærke nok til at holde molekyler sammen ved 32°F, men alligevel svage nok til at det smelter igen ved 32°F (0°C). Denne balance giver vandet dets unikke frysetemperatur.
Frysepunktsdepression med opløste stoffer
Tilsætning af stoffer som sukker, salt eller alkohol sænker temperaturen, hvor vandet fryser. Jo mere opløst stof du tilføjer, jo større fald. Det er derfor, vejpersonalet spreder salt på iskolde fortove - salt sænker frysepunktet og forvandler is til flydende vand, selv når temperaturen ligger lige under 32°F. På samme måde forbliver vodka, som indeholder omkring 40 % ethanol, flydende i en standardfryser, fordi alkohols tilstedeværelse sænker frysepunktet med flere grader.
Isdannelse, udvidelse og krystalstrukturer
De fleste materialer trækker sig sammen, når de afkøles, men vand opfører sig anderledes. Den når maksimal tæthed ved omkring 39°F (4°C). Herunder udvider vandet sig, når dets molekyler vedtager et sekskantet gitter, hvilket skaber huller, der gør is mindre tæt end flydende vand. Denne udvidelse er årsagen til, at snefnug dannes, da det sekskantede arrangement fortsætter med at vokse til sarte krystaller.
Presset fra ekspanderende is
Fordi is udvider sig, kan en forseglet beholder med vand briste, når den fryses. Trykket, der udøves af ekspanderende is, kan nå op til 40.000 psi ved –7,6 °F (–22 °C). Selv robuste beholdere, såsom stål eller jern, kan svigte under denne stress, hvorfor du ofte vil se flasker sprænge i fryseren.
Sidste artikelBeregning af ligevægtstryk:En trin-for-trin guide
Næste artikelSyrer vs. baser:Vigtige kemiske forskelle forklaret
 Varme artikler
Varme artikler
-
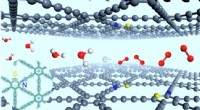 Forskere udvikler stereodefineret N- og S-atom-kodoperet grafdiyn til iltudviklingStereodefinerede sp-N- og S-atomer til effektiv iltudvikling. Kredit:Zhao Yasong Iltudviklingsreaktionen (OER) er af stor betydning i energirelaterede teknikker såsom metal-luft-batterier og vands
Forskere udvikler stereodefineret N- og S-atom-kodoperet grafdiyn til iltudviklingStereodefinerede sp-N- og S-atomer til effektiv iltudvikling. Kredit:Zhao Yasong Iltudviklingsreaktionen (OER) er af stor betydning i energirelaterede teknikker såsom metal-luft-batterier og vands -
 En balancegang:Forbedret vandbehandlingsteknik ved hjælp af energitilpasningMangel på ferskvand i mange dele af verden kræver forbedrede og bæredygtige metoder til spildevandsrensning. Kredit:PS Photography på Pexels I dag, et stort antal mennesker verden over lider under
En balancegang:Forbedret vandbehandlingsteknik ved hjælp af energitilpasningMangel på ferskvand i mange dele af verden kræver forbedrede og bæredygtige metoder til spildevandsrensning. Kredit:PS Photography på Pexels I dag, et stort antal mennesker verden over lider under -
 Ny kemisk metode gør det lettere at ekstrahere forurenende pesticider fra vandKredit:Asociacion RUVID Forskere fra Institut for Analytisk Kemi og Institute of Materials Science (ICMUV) ved University of Valencia (UV) har udviklet en metode til påvisning i vand af PFRer (org
Ny kemisk metode gør det lettere at ekstrahere forurenende pesticider fra vandKredit:Asociacion RUVID Forskere fra Institut for Analytisk Kemi og Institute of Materials Science (ICMUV) ved University of Valencia (UV) har udviklet en metode til påvisning i vand af PFRer (org -
 Maskinlæring tilbyder en ny måde at designe kirale krystaller påFor at bygge en chiral magnet (billedet), det er nødvendigt først at designe en chiral krystal. Kredit:Julien Zaccaro / Center for Chiral Science Ingeniører og kemikere ved Hiroshima University ha
Maskinlæring tilbyder en ny måde at designe kirale krystaller påFor at bygge en chiral magnet (billedet), det er nødvendigt først at designe en chiral krystal. Kredit:Julien Zaccaro / Center for Chiral Science Ingeniører og kemikere ved Hiroshima University ha
- Hvordan beskriver du bevægelsen af primære bølger?
- Hvad kredserer Galaxy Orbit, hvis noget?
- Hvad er to hovedkomponenter i cytoplasmaet?
- Endpoint Math Formel
- Hvorfor kaldes NASAS -projekt uden for Jorden Origins?
- Hvad er energien fra en elektromagnetisk bølge med frekvens 8 og gange10 til 12. effekt Hz?


