Beregning af ligevægtstryk:En trin-for-trin guide
Af Lee Johnson • Opdateret 24. marts 2022
Kemisk ligevægt beskriver den stabile tilstand af en reversibel reaktion, hvor reaktanter omdannes til produkter og omvendt med lige store hastigheder. I praksis kvantificerer kemikere denne balance ved hjælp af ligevægtskonstanten, Kp , som forbinder partialtrykket af de involverede gasser.
Forstå ligevægtskonstanten
For en generisk gasfasereaktion:
\(aA(g)+bB(g)\rightleftharpoons cC(g)+dD(g)\)
ligevægtskonstanten er defineret som:
\(K_p =\frac{(P_C)^c(P_D)^d}{(P_A)^a(P_B)^b}\)
Når alle støkiometriske koefficienter er lig med én, forenkles udtrykket til "produkter over reaktanter." Denne formular er kun gyldig ved ligevægt.
Nogle gange vil du se ligevægtskonstanten udtrykt i molære koncentrationer, Kc , relateret til Kp af:
\(K_p =K_c (RT)^{\Delta n}\)
hvor Δn er ændringen i antallet af gasmol mellem produkter og reaktanter.
Omarrangering af ligningen for at finde ligevægtstryk
Nøgletrinet er at introducere variablen x , som repræsenterer ændringen i tryk fra startværdien til ligevægt. Antag, at starttrykket for hver reaktant er P_i og produkterne starter ved nul tryk. Derefter kan hvert ligevægtstryk udtrykkes i x .
Med alle koefficienter sat til én, er Kp udtryk bliver:
\(\begin{aligned}K_p &=\frac{x^2}{(P_i - x)^2}\end{aligned}\)
Løsning for x giver:
\(x =\frac{\sqrt{K_p}\,P_i}{1 + \sqrt{K_p}}\)
Ligevægtspartialtrykket for en reaktant er P_i - x , mens det for et produkt blot er x .
Eksempel:Fremstilling af klormethan
Overvej reaktionen:
\(\tekst{CH}_3\text{OH(g)} + \text{HCl(g)} \rightleftharpoons \text{CH}_3\text{Cl(g)} + \text{H}_2\text{O(g)}\)
Med Kp =5{}900 og et starttryk P_i =0,75 atm for hver reaktant, beregne x :
\(\begin{aligned} x &=\frac{\sqrt{K_p}\,P_i}{1 + \sqrt{K_p}} \\ &=\frac{\sqrt{5900}\times 0,75\;\text{atm}}{1 + \sqrt{5900}} 0,74\;\text{atm}\end{aligned}\)
Således er ligevægtstrykket for hvert produkt omkring 0,74 atm, og trykket for hver reaktant er 0,75 - 0,74 =0,01 hæveautomat.
Ved at følge denne systematiske tilgang kan du nøjagtigt bestemme ligevægtstryk for enhver gasfasereaktion.
 Varme artikler
Varme artikler
-
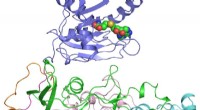 Forskere knækker strukturen af nøgleprotein i Zika-virusKrystalstrukturen af ZIKV NS5-protein. Regionerne med forskellige farver repræsenterer individuelle domæner eller motiver af ZIKV NS5. Den sorte cirkel markerer placeringen af det potentielle inhi
Forskere knækker strukturen af nøgleprotein i Zika-virusKrystalstrukturen af ZIKV NS5-protein. Regionerne med forskellige farver repræsenterer individuelle domæner eller motiver af ZIKV NS5. Den sorte cirkel markerer placeringen af det potentielle inhi -
 Forskere fanger øjeblikke med spirende krystaldannelse og vækstFoto af en guldkrystal. Kredit:© Paul Straathof/Pauls Lab Omdannelse af de fleste materialer til organiseret krystallinsk struktur starter med nukleationsprocessen. Et daglig eksempel er den hurti
Forskere fanger øjeblikke med spirende krystaldannelse og vækstFoto af en guldkrystal. Kredit:© Paul Straathof/Pauls Lab Omdannelse af de fleste materialer til organiseret krystallinsk struktur starter med nukleationsprocessen. Et daglig eksempel er den hurti -
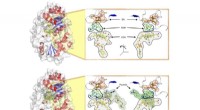 Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala
Hvordan et bestemt protein regulerer op til to tredjedele af verdens metanudledningOverfladeillustrationer af enzymet Mmp10, der viser (øverst) proteinet med det komplette sæt af co-faktorer, der kræves for at den enzymatiske reaktion kan forekomme (nemlig:SF4-klyngen, SAM og cobala -
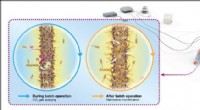 Multifunktionelle porøse ledende membraner hjælper mikrober med at spise sig frem til en hurtigere…Illustration af den mikrobielle elektrosynteseproces, hvorved levende mikrober omdanner kuldioxid til nyttige kemikalier i en elektrokemisk celle via en reduktionsreaktion under påført spænding. Kredi
Multifunktionelle porøse ledende membraner hjælper mikrober med at spise sig frem til en hurtigere…Illustration af den mikrobielle elektrosynteseproces, hvorved levende mikrober omdanner kuldioxid til nyttige kemikalier i en elektrokemisk celle via en reduktionsreaktion under påført spænding. Kredi
- Bruger ALMA til at løse solens koronale varmemysterium
- Tilfældige processer former videnskab og matematik:Forskere foreslår en samlet, probabilistisk ram…
- Forfædres skøn fastholder racisme, hvid overmagt
- Bruges DNA til at identificere genetiske lidelser?
- Nye værktøjer til at skabe spejlede former for molekyler
- Hvor lang tid ville det tage lys at rejse fra den nærmeste stjerne USA?


