Nye værktøjer til at skabe spejlede former for molekyler

Gregory Fu og Zhaobin Wang hos Caltech. Kredit:Caltech
En af de største udfordringer, som syntetiske kemikere står over for, er, hvordan man laver molekyler af kun en bestemt "håndhævelse". Molekyler kan komme i to former, der spejler hinanden, ligesom vores venstre og højre hånd. Denne egenskab, kaldet chiralitet, kan findes i biologiske molekyler som sukker og proteiner, hvilket betyder, at lægemiddeldesignere ofte ønsker at udvikle medicin, der kun er venstre- eller højrehåndet. Det er lidt ligesom at designe det ideelle håndtryk.
Kemikere har udviklet måder at adskille venstre- og højrehåndede former, eller enantiomerer, af et molekyle - såsom molekylsigter, der tillader passage af kun én form. En anden mere efterspurgt teknik er at skabe, fra starten, kun den ønskede enantiomer og ikke dens spejlbillede. I en ny undersøgelse, udgivet 18. oktober i Natur , Gregory Fu, Caltechs Norman Chandler professor i kemi, og hans team gør netop det, demonstrerer en ny metode til fremstilling af molekyler med carbon-carbon-bindinger (stort set alle lægemidler indeholder carbon-carbon-bindinger) i kun en af deres håndformer, mens du bruger rigeligt, billige materialer.
"Denne metode kan gøre opdagelsen og syntesen af bioaktive forbindelser, såsom lægemidler, billigere og mindre tidskrævende end det var muligt med tidligere metoder, " siger Fu. "En lægemiddeludvikler kunne bruge vores metode til lettere at lave biblioteker af kandidatlægemidler, som de så ville teste for en ønsket aktivitet."
I den nye rapport, forskerne demonstrerer, at de kan køre deres håndvalgsreaktioner ved hjælp af billige materialer, inklusive en nikkelkatalysator, et alkylhalogenid, et siliciumhydrid, og en olefin. Olefiner er molekyler, der indeholder carbon-carbon dobbeltbindinger, og de findes almindeligvis i organiske molekyler. I 2005, Bob Grubbs, Victor og Elizabeth Atkins professor i kemi ved Caltech, vandt Nobelprisen i kemi for at finde på en metode til at bytte atomer ind og ud af olefiner efter behag, et fund, der førte til bedre måder at fremstille olefiner til industrielle formål.
Fu-teamet skabte forskellige klasser af forbindelser med en specifik chiralitet, herunder molekyler kendt som beta-lactamer, hvoraf antibiotikumet penicillin er medlem.
"Nikkelkatalysatorerne fungerer som en form af en handske, forme et molekyle til den ønskede venstre eller højre hånd. Du kunne, i teorien, bruge vores metode til lettere at lave en række penicillin-lignende molekyler, for eksempel, " siger Fu.
Molekyler med forskellig håndhed kan have overraskende forskellige træk. Det kunstige sødemiddel aspartam har to enantiomerer - den ene smager sødt, mens den anden ikke smager. Molekylet carvone lugter som grøn mynte i den ene form og som kommen i den anden. Lægemidler kan også have forskellige virkninger afhængigt af deres håndhævelse. Ibuprofen, også kendt under et af sine mærkenavne, Advil, indeholder både venstre- og højrehåndede former, men kun én version er terapeutisk.
I fremtiden, Fu og hans kolleger planlægger at videreudvikle deres metode - især de ønsker at være i stand til at kontrollere håndenheden på to steder i et molekyle i stedet for kun ét, give lægemiddeldesignere endnu mere fleksibilitet.
Undersøgelsen har titlen, "Katalytisk enantiokonvergent kobling af sekundære og tertiære elektrofiler med olefiner."
 Varme artikler
Varme artikler
-
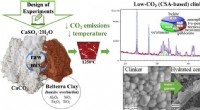 Alternativ cement med lavt CO2-fodaftryk udvikletGrafisk abstrakt. Kredit:DOI:10.1016/j.susmat.2021.e00299 Forskere ved Martin Luther University Halle-Wittenberg (MLU) i Tyskland og det brasilianske universitet i Pará har udviklet et klimavenlig
Alternativ cement med lavt CO2-fodaftryk udvikletGrafisk abstrakt. Kredit:DOI:10.1016/j.susmat.2021.e00299 Forskere ved Martin Luther University Halle-Wittenberg (MLU) i Tyskland og det brasilianske universitet i Pará har udviklet et klimavenlig -
 At lære nye tricks fra havsvampe, naturens mest usandsynlige civilingeniørerGlasfibrene, der udgør Euplectella aspergillum-svampen, er overraskende stærke og fleksible. Kredit:Michael A Monn, CC BY-ND Forestil dig en fremtid, hvor bygninger knejser kilometervis over gader
At lære nye tricks fra havsvampe, naturens mest usandsynlige civilingeniørerGlasfibrene, der udgør Euplectella aspergillum-svampen, er overraskende stærke og fleksible. Kredit:Michael A Monn, CC BY-ND Forestil dig en fremtid, hvor bygninger knejser kilometervis over gader -
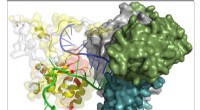 Forskere undersøger strukturen i en nøgleregion af langtidsprotein -telomeraseModel af telomerase katalytisk underenhed af H. polymorpha med fragmenter af telomerase RNA og telomert DNA. Rester, der deltager i bindingen af oligonukleotider, er markeret med rødt i TED-domæne
Forskere undersøger strukturen i en nøgleregion af langtidsprotein -telomeraseModel af telomerase katalytisk underenhed af H. polymorpha med fragmenter af telomerase RNA og telomert DNA. Rester, der deltager i bindingen af oligonukleotider, er markeret med rødt i TED-domæne -
 Kortlægning af solcellernes energiske landskabKredit:CC0 Public Domain En ny spektroskopisk metode gør det nu muligt at måle og visualisere det energiske landskab inde i solceller baseret på organiske materialer. Det blev udviklet af et forsk
Kortlægning af solcellernes energiske landskabKredit:CC0 Public Domain En ny spektroskopisk metode gør det nu muligt at måle og visualisere det energiske landskab inde i solceller baseret på organiske materialer. Det blev udviklet af et forsk
- Isbjerge, der driver fra Canada til det sydlige Florida
- En rhodiumbaseret katalysator til fremstilling af organosilicium ved hjælp af mindre ædle metaller
- Forskere måler den udviklende energi af et soludbrudseksplosiv de første minutter
- Ny undersøgelse undersøger funktionalitet i akvatiske økosystemer
- Klimaændringer gør byggeri, fiskeri og andre farlige industrier endnu mere risikable
- Investorer kunne pumpe 1 mia. Dollar ind i Uber selvkørende biler:rapporter


