Reaktionsstøkiometri:Udforskning af reaktant- og produktrelationer
1. Moleforhold og balanceringsligninger:
* Afbalancering af kemiske ligninger: Dette sikrer, at antallet af atomer i hvert element er det samme på begge sider af ligningen, hvilket repræsenterer loven om bevarelse af masse.
* Muldvarpeforhold: Koefficienterne i en afbalanceret kemisk ligning repræsenterer molforholdet mellem reaktanter og produkter. Dette forhold hjælper med at bestemme, hvor mange mol af et stof, der skal til for at reagere fuldstændigt med et givet antal mol af et andet.
2. Masseforhold:
* Molar masse: Molmassen af et stof er massen af et mol af det pågældende stof.
* Masse-til-masse-konverteringer: Ved hjælp af molær masse og molforhold kan du beregne massen af reaktanter eller produkter involveret i en reaktion. For eksempel, givet massen af en reaktant, kan du beregne massen af det dannede produkt.
3. Begrænsning af reaktant og procentudbytte:
* Begrænsende reaktant: Reaktanten, der forbruges fuldstændigt først i en reaktion. Det bestemmer den maksimale mængde produkt, der kan dannes.
* Procentudbytte: Forholdet mellem det faktiske udbytte (mængden af opnået produkt) og det teoretiske udbytte (mængden af produkt beregnet ud fra støkiometri), udtrykt i procent. Dette hjælper med at vurdere effektiviteten af en reaktion.
4. Andre faktorer:
* Løsningsstøkiometri: Behandler reaktioner, der forekommer i opløsninger, involverer begreber som molaritet og volumen.
* Gasstøkiometri: Fokuserer på reaktioner, der involverer gasser, i betragtning af den ideelle gaslov og gasvolumener ved standardbetingelser.
Sammenfattet er reaktionsstøkiometri grundlaget for at forstå og forudsige mængderne af stoffer involveret i kemiske reaktioner. Denne viden er afgørende på forskellige områder, herunder:
* Kemiforskning: Design af eksperimenter og analyse af resultater.
* Kemiteknik: Optimering af industrielle processer og opskalering af produktion.
* Miljøvidenskab: Forudsige virkningen af kemiske reaktioner på miljøet.
* Medicin og apotek: Udvikling og fremstilling af lægemidler og andre lægemidler.
 Varme artikler
Varme artikler
-
 Saltsyre:Sikkerhedsretningslinjer for håndtering, transport og opbevaringAf Percila Jackson Opdateret 24. marts 2022 Saltsyre (HCl) er et stærkt ætsende stof, når det er koncentreret. Korrekte sikkerhedsforanstaltninger er afgørende ved håndtering, transport og opbevarin
Saltsyre:Sikkerhedsretningslinjer for håndtering, transport og opbevaringAf Percila Jackson Opdateret 24. marts 2022 Saltsyre (HCl) er et stærkt ætsende stof, når det er koncentreret. Korrekte sikkerhedsforanstaltninger er afgørende ved håndtering, transport og opbevarin -
 Forskere rapporterer nyt, mere effektiv katalysator til vandspaltningKredit:George Hodan/public domain Fysikere fra University of Houston har opdaget en katalysator, der kan opdele vand i brint og ilt, består af let tilgængelige, billige materialer og fungerer lang
Forskere rapporterer nyt, mere effektiv katalysator til vandspaltningKredit:George Hodan/public domain Fysikere fra University of Houston har opdaget en katalysator, der kan opdele vand i brint og ilt, består af let tilgængelige, billige materialer og fungerer lang -
 Er det hamp eller marihuana? Ny scanner giver øjeblikkeligt svarHovedforfatter Lee Sanchez scanner et hampblad for THC, demonstrerer en af de snesevis af scanninger, han skulle udføre for at perfektionere holdets metode. Kredit:Dmitry Kurouski Hamp er teknis
Er det hamp eller marihuana? Ny scanner giver øjeblikkeligt svarHovedforfatter Lee Sanchez scanner et hampblad for THC, demonstrerer en af de snesevis af scanninger, han skulle udføre for at perfektionere holdets metode. Kredit:Dmitry Kurouski Hamp er teknis -
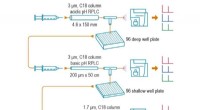 Forbedret proteinanalyse kan hjælpe med tidlig sygdomsdetektionPNNLs dybdyk-SRM-metode tilbyder en ny måde at forberede og analysere blodprøver på, og gør det muligt at påvise proteiner, der findes i meget lave koncentrationer – så lidt som 10 pikogram pr. millil
Forbedret proteinanalyse kan hjælpe med tidlig sygdomsdetektionPNNLs dybdyk-SRM-metode tilbyder en ny måde at forberede og analysere blodprøver på, og gør det muligt at påvise proteiner, der findes i meget lave koncentrationer – så lidt som 10 pikogram pr. millil
- Ny Hubble konstant måling tilføjer mysteriet om universets ekspansionshastighed
- I genetik Hvad er de kvindelige sexkromosomer?
- Kvantefangen, et gratis videnskabeligt og teknologisk videospil er nu tilgængeligt online
- Hvordan er bevægelser af planter forskellige hos dyr?
- Hvor mange cm og i et pund?
- Hvad er tvetydigt tilfælde af synderetten?


