Beregn pH-værdien af en 0,15 M calciumhydroxidopløsning:Trin-for-trin-vejledning
1. Forstå dissociationen:
Calciumhydroxid (Ca(OH)2) er en stærk base. Det dissocierer fuldstændigt i vand:
Ca(OH)₂ (vandig) → Ca²⁺ (vandig) + 2OH⁻ (vandig)
Det betyder, at for hver 1 mol Ca(OH)₂, der opløses, får du 2 mol hydroxidioner (OH⁻).
2. Beregn hydroxidionkoncentrationen:
* Da koncentrationen af Ca(OH)2 er 0,15 M, er koncentrationen af OH⁻-ioner det dobbelte:0,15 M * 2 =0,30 M
3. Beregn pOH:
pOH er den negative logaritme af hydroxidionkoncentrationen:
pOH =-log[OH⁻] =-log(0,30) ≈ 0,52
4. Beregn pH:
pH og pOH er forbundet med følgende ligning:
pH + pOH =14
Derfor:
pH =14 - pOH =14 - 0,52 ≈ 13,48
Derfor er pH-værdien af en 0,15 M calciumhydroxidopløsning ca. 13,48.
Sidste artikelForstå det grundlæggende ved calciumoxidopløsninger
Næste artikelForstå regnvandets pH:hvorfor det er surt (under 7)
 Varme artikler
Varme artikler
-
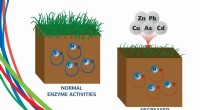 Tungmetaller gør jordens enzymer 3 gange svagereTungmetaller gør jordens enzymer 3 gange svagere, Siger en jordforsker fra RUDN University. Kredit:RUDN University Tungmetaller undertrykker enzymaktivitet i jorden tre til 3,5 gange og har særlig
Tungmetaller gør jordens enzymer 3 gange svagereTungmetaller gør jordens enzymer 3 gange svagere, Siger en jordforsker fra RUDN University. Kredit:RUDN University Tungmetaller undertrykker enzymaktivitet i jorden tre til 3,5 gange og har særlig -
 Tyndhudede solpaneler printet med inkjetDen fuldt printede ultratynde solcelle er let og fleksibel nok til at hvile på overfladen af en sæbeboble. Kredit:2020 KAUST; Anastasia Serin Solceller kan nu laves så tynde, lette og fleksible,
Tyndhudede solpaneler printet med inkjetDen fuldt printede ultratynde solcelle er let og fleksibel nok til at hvile på overfladen af en sæbeboble. Kredit:2020 KAUST; Anastasia Serin Solceller kan nu laves så tynde, lette og fleksible, -
 Nye glasmaterialer fremstillet af organiske og uorganiske komponenterDr. Courtney Calahoo fra University of Jena præsenterer organisk glas (l.) og uorganisk glas (r.) - to udgangsmaterialer til det nye kompositglas. Kredit:Jens Meyer/University of Jena Cambridge/Je
Nye glasmaterialer fremstillet af organiske og uorganiske komponenterDr. Courtney Calahoo fra University of Jena præsenterer organisk glas (l.) og uorganisk glas (r.) - to udgangsmaterialer til det nye kompositglas. Kredit:Jens Meyer/University of Jena Cambridge/Je -
 Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
Solar fordamper tilbyder en frisk rute til ferskvandEn selvrensende anordning lavet af træ har til formål at gøre småskala afsaltning mere praktisk. Kredit:John T. Consoli/University of Maryland Omkring en milliard mennesker verden over mangler adg
- Er solenergi vind og geotermisk uudtømmelig ressource?
- Magnetisk hud sikrer, at kraften er med dig
- Polymer SunBOT'er efterligner solsikker for at skabe maksimal solenergi
- Hvorfor findes petroleum altid i et område med sedimentær klippe?
- Jordens nedre kappe kan oxideres i nærvær af vand
- Områder i verden, der har sedimentære klipper


