Forstå regnvandets pH:hvorfor det er surt (under 7)
Her er hvorfor:
* CO2 opløses i vand: Når kuldioxid fra atmosfæren opløses i vand, danner det kulsyre (H2CO3).
* Carbonsyre dissocierer: Kulsyre opløses derefter i hydrogenioner (H+) og bicarbonationer (HCO3-).
* Brintioner øger surhedsgraden: Tilstedeværelsen af brintioner i regnvandet øger dets surhedsgrad, hvilket resulterer i en pH lavere end 7.
De kemiske reaktioner er som følger:
CO2(g) + H2O(l) ⇌ H2CO3(aq)
H2CO3(aq) ⇌ H+(aq) + HCO3-(aq)
Derfor er regnvandets pH-værdi naturligt let sur på grund af den opløste kuldioxid.
Det er dog vigtigt at bemærke, at:
* Sur regn: Regnvand kan blive væsentligt surere (pH under 5,6) på grund af luftforurening fra menneskelige aktiviteter, såsom afbrænding af fossile brændstoffer. Dette skyldes, at forurenende stoffer som svovldioxid (SO2) og nitrogenoxider (NOx) reagerer med vand og danner svovlsyre (H2SO4) og salpetersyre (HNO3), som yderligere sænker pH.
* Naturlige variationer: Regnvandets pH kan variere afhængigt af faktorer som placering, temperatur og tilstedeværelsen af andre atmosfæriske gasser.
Samlet set, mens regnvand naturligt har en svagt sur pH på grund af opløst CO2, kan menneskelige aktiviteter bidrage væsentligt til sur regn, hvilket fører til alvorlige miljømæssige konsekvenser.
 Varme artikler
Varme artikler
-
 Ikke-forurenende membran til overtøjDe unge iværksættere Anna Beltzung og Mario Stucki er i startskuddet med deres membraner. Kredit:ETH Zürich / Peter Rüegg Som en del af sit kandidatprojekt, kemiingeniøren Mario Stucki udviklede e
Ikke-forurenende membran til overtøjDe unge iværksættere Anna Beltzung og Mario Stucki er i startskuddet med deres membraner. Kredit:ETH Zürich / Peter Rüegg Som en del af sit kandidatprojekt, kemiingeniøren Mario Stucki udviklede e -
 Kemikere bruger modificerede DNA -nukleotider til at skabe nye materialerDiagram over enzym (orange) indkapslende 2-azido-DNA/DNA hydrogel. Kredit:Romesberg Lab DNA udviklede sig til at gemme genetisk information, men i princippet denne særlige, kædelignende molekyle k
Kemikere bruger modificerede DNA -nukleotider til at skabe nye materialerDiagram over enzym (orange) indkapslende 2-azido-DNA/DNA hydrogel. Kredit:Romesberg Lab DNA udviklede sig til at gemme genetisk information, men i princippet denne særlige, kædelignende molekyle k -
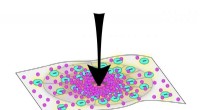 Under pres:Nyt bioinspireret materiale kan formskifte til eksterne kræfterTil JHU-teamets eksperiment, øget kraft (pilen peger nedad) påført materialet førte til flere elektriske ladninger, og dermed, mere mineralisering. Kredit:Pam Li/Johns Hopkins University Inspirere
Under pres:Nyt bioinspireret materiale kan formskifte til eksterne kræfterTil JHU-teamets eksperiment, øget kraft (pilen peger nedad) påført materialet førte til flere elektriske ladninger, og dermed, mere mineralisering. Kredit:Pam Li/Johns Hopkins University Inspirere -
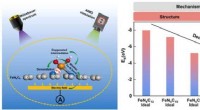 Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne
Forskere afslører nedbrydningsmekanismen for ikke-ædelmetalkatalysatorer til brændselscellerGrafisk abstrakt. Kredit:Anvendt katalyse B:Miljø (2022). DOI:10.1016/j.apcatb.2022.121290 Udviklingen af effektive ikke-ædelmetalkatalysatorer (NPMCer) kan hjælpe med at reducere omkostningerne
- Hvordan øger uafhængig orientering af kromosom under meiose genetisk variation?
- Hvad er rækkefølgen af størrelseslængde en blyant i tommer?
- Klippen mest sandsynligt at indeholde fossiler
- Den proces, hvormed celler nedbryder enkle madmolekyler for at frigive energi, de indeholder?
- Mikroskop hjælper med dinosaurpuslespil
- Hvorfor er det lettere at gå gennem en gammel moden skov med høje træer end en unge små træer?


